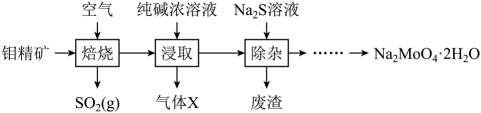
已知:浸取液溶质主要为和
。

已知:镉(Cd)的金属活动性介于锌、铁之间。下列说法错误的是( )
| 选项 | 物质 | 除杂试剂 | 分离方法 |
| A | 二氧化硅(碳酸钙) | 氢氧化钠溶液 | 过滤 |
| B | 硫酸铜溶液(硫酸铁) | 加入过量铜粉 | 过滤 |
| C | 乙醇(乙酸) | 生石灰 | 蒸馏 |
| D | SO2(CO2) | 碳酸钠溶液 | 洗气 |

下列说法正确的是( )

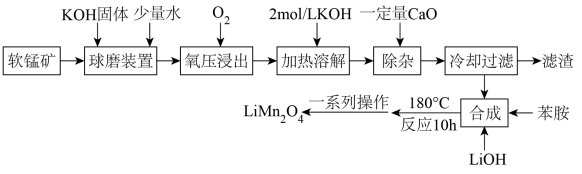
已知:
①软锰矿的成分如下:
|
成分 |
MnO2 |
Fe2O3 |
CaO |
SiO2 |
其他不反应杂质 |
|
质量分数 |
69.6% |
7.6% |
5.6% |
9.0% |
8.2% |
②K2MnO4在强碱性溶液(pH大于13.5)中稳定,在酸性、中性和弱碱性环境中会发生歧化反应生成和MnO2。
③苯胺(C6H5NH2)还原性较强,在该条件下可被氧化为硝基苯(C6H5NO2)。
④锰酸锂为灰黑色粉末,离子化合物,易溶于水,难溶于无水乙醇。
①若反应时,N元素的化合价不变,则锰酸锂与稀硝酸和双氧水反应的离子方程式为。
②样品中锰酸锂的纯度为%(保留两位有效数字)。

已知:①单宁酸是一种只含C、H、O元素的有机化合物
② , 常温下
,
,
,
③当溶液中某离子的物质的量浓度不大于时,该离子沉淀完全


已知几种金属阳离子的氢氧化物沉淀时的pH如下表:
金属阳离子 | ||||
开始沉淀时pH | 1.5 | 3.3 | 6.5 | 5.2 |
沉淀完全时pH | 3.7 | 5.0 | 9.7 | — |
①基态的最高能层中成对电子与未成对电子的数目之比为。
②重铬酸铵常用作有机合成催化剂,
的结构如图。
中
键数目为
。

![]()
已知:①含锌组分间的转化关系:Zn2+Zn(OH)2
②ε−Zn(OH)2是Zn(OH)2的一种晶型,39℃ 以下稳定。
请回答:
仪器: a.烧杯 b.托盘天平 c.容量瓶 d.分析天平 e.试剂瓶

 已知:①
已知:① 微溶于水,它的溶解度随温度升高而逐渐增大,且能与过量的
离子生成
而溶解。②浸出液A含有大量
及少量
金属离子。

 ①用化学用语和适当的文字说明:随
①用化学用语和适当的文字说明:随 比值的增加,钴的沉淀率先逐渐增大后又逐渐减小的原因是。
②沉淀反应时间为 ,温度在
以下时,随着温度的升高,钻的沉淀率升高的可能原因是。

已知:①有关金属离子形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
| 开始沉淀的pH | 7.5 | 2.7 | 5.6 | 8.3 |
| 完全沉淀的pH | 9.0 | 3.7 | 6.7 | 9.8 |
②[Cu(NH3)4]SO4常温稳定,在热水中会分解生成NH3;
③Ksp[Fe(OH)3]=4.0×10-8。
回答下列问题:

有关物质的性质如下表所示:
| 甘氨酸(H2NCH2COOH) | 易溶于水,能溶于冰醋酸,难溶于乙醇、乙醚,水溶液呈弱酸性。 |
| 柠檬酸 | 易溶于水和乙醇,酸性较强,有强还原性。 |
| 甘氨酸亚铁 | 易溶于水且在水中难电离,难溶于乙醇、冰醋酸。 |
实验步骤如下:
Ⅰ.打开K1、K3 , 向c中通入气体,待确定c中空气被排尽后,将b中溶液加入到c中。
Ⅱ.在50℃恒温条件下用磁力搅拌器不断搅拌,然后向c中滴加适量NaOH溶液调溶液pH至5.5左右,使反应物充分反应。
Ⅲ.反应完成后,向c中加入无水乙醇,析出沉淀,过滤、洗涤得粗产品,将粗产品纯化后得精品。
回答下列问题:
①将粗产品溶于一定量的冰醋酸中,经搅拌,,洗涤,将滤液配成100.00mL的溶液,移取25.00mL溶液于锥形瓶,进行滴定。
②滴定过程中下列操作会使甘氨酸测定结果偏高的是(填字母)。
A.滴定时未用高氯酸标准溶液润洗滴定管
B.读数时,滴定前平视,滴定终点时俯视
C.摇动锥形瓶时有液体溅出
D.滴定前滴定管尖嘴处有气泡,滴定后消失
①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
②反应过程中C2H5OH和HCl可能会生成副产物C2H5Cl,同时CCl3CHO(三氯乙醛)也能被次氯酸继续氧化生成CCl3COOH(三氯乙酸)
③相关物质的相对分子质量及部分物理性质:
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | |
| C2H5OH | 46 | ﹣114.1 | 78.3 | 与水互溶 |
| CCl3CHO | 147.5 | ﹣57.5 | 97.8 | 可溶于水、乙醇 |
| CCl3COOH | 163.5 | 58 | 198 | 可溶于水、乙醇、三氯乙醛 |
| C2H5Cl | 64.5 | ﹣138.7 | 12.3 | 微溶于水,可溶于乙醇 |
 +CH3COOH
+CH3COOH
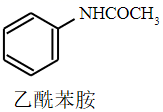 +H2O
+H2O
乙酸、苯胺、乙酰苯胺的部分物理性质如下表
| 乙酸 | 苯胺 | 乙酰苯胺 | |
| 沸点 | 118 | 184 | 304 |
| 状态 | 无色液体 | 无色液体 | 白色固体 |
| 在水中的溶解度 | 易溶于水 | 易溶于水20℃溶解度3.6g | 20℃溶解度0.46g;80℃溶解度3.5g;100C溶解度18g |
实验过程:①在50mL蒸馏瓶中加入沸石、乙酸7.4mL(过量),苯胺5mL,实验装置如下图所示(加热装置略去),先小火加热10分钟,再控制分馏柱温度为105℃,加热至反应完成。

②趁热将反应后的混合物倒入装有100mL冷水的烧杯中,快速搅拌,用布氏漏斗抽滤。
③洗涤沉淀、再抽滤得固体,检验乙酰苯胺中的乙酸是否被除尽。
④将沉淀转移到表面皿上,加热蒸发,除去水。
回答下列问题:

相关物质的数据及性质如下表:
| 主要性状 | 熔点/℃ | 沸点/℃ | 主要化学性质 | |
| SOCl2 | 淡黄至红色发烟液体 | -105 | 78.8 | 遇水分解, 140℃开始分解 |
| S2Cl2 | 浅黄色油状液体 | -80 | 138 | 遇水分解,高于100℃时开始分解 |
回答下列问题:


实验操作如下:关闭f,打开e,然后关闭活塞a,打开活塞b、c,加入适量稀硫酸反应一段时间后,关闭活塞b、c,打开活塞a,以上操作的目的是;实验结束后,若装置B中没有出现碳酸亚铁晶体,可能的原因是。
实验操作如下:将装置1制取的碳酸亚铁晶体与甘氨酸的水溶液混合加入C中,关闭e,打开f,然后利用E中盐酸和碳酸钙反应生成的气体排尽装置中的空气,接着滴入柠檬酸溶液并加热。反应结束后过滤,滤液经蒸发结晶、过滤、洗涤、干燥,得到甘氨酸亚铁。
仪器h的名称为;试剂g为(填试剂名称)。

已知:TiO2不与碱反应,与酸反应后以TiO2+的形式存在。回答下列问题:
海带 海带灰
海带灰浸取液
取海带灰浸取液 ,加入稀硫酸约
、5%的
溶液约
,然后加入
约
,振荡后静置,可以观察到,证明海带中含有碘元素,该反应的离子方程式为。
海带灰浸取液 含I2的水溶液
碘的有机溶液→晶体碘
若向 碘水L中加入
,充分振荡、静置,此时碘在
中的物质的量浓度是水中的86倍,则萃取效率为%(结果保留小数点后两位)(萃取效率
)。

若称取干海带 ,经灼烧、浸取、
氧化等过程后配制成
溶液,移取
于锥形瓶中,用
标准溶液滴定,待溶液由黄色变为浅黄色时,滴加两滴淀粉指示剂,继续滴定至蓝色刚好褪去,且半分钟内无变化,即为终点,平行滴定3次,记录所消耗的
溶液的平均体积为
,计算海带中含碘的质量分数为%(结果保留小数点后两位)(已知
)。若滴定结束读数时俯视刻度线,会导致测定结果(填“偏高”“偏低”或“不影响”)。

为了提高磁选效率,可采取的措施为。

熔炼过程中反应的化学方程式为,熔炼过程中发生的反应为吸热反应,该反应能够自发进行的原因是。
Ⅲ.从 获得单质钛也可以采用熔盐电解法,“熔盐电解法”被认为是最可能全面代替“金属热还原法”的工艺。FFC-熔盐电脱氧法的具体流程为:将二氧化钛压制成型,经过预烧结,制备成电解体系的阴极,石墨作惰性阳极,以氯化钠、氯化钙为混合熔盐,在低于一定电压条件下(熔盐不分解)电解,阴极生成金属钛。

已知:
I:Cr(OH)3和Zn(OH)2是两性氢氧化物
II:室温下,Ni(OH)2的Ksp约为1.0×10-15
回答下列问题:

 )在工业上作磺胺类药物原料等,可通过苯胺和乙酸反应制得:
)在工业上作磺胺类药物原料等,可通过苯胺和乙酸反应制得: 已知:纯乙酰苯胺是白色片状晶体,熔点为114℃;微溶于冷水,可溶于热水,易溶于有机溶剂;加热时易被氧化。
实验室制备乙酰苯胺的步骤如下(部分装置省略):
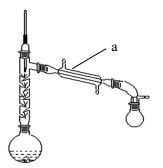
Ⅰ.粗乙酰苯胺的制备
在150mL 烧瓶中加入15mL(过量)乙酸(沸点117.9℃)、少量Zn粉和10mL(0.11mol)新制得的苯胺,如图接好装置。在石棉网上用小火加热,控制顶端馏出温度105℃左右使之充分反应1h。待反应完成,在不断搅拌下,趁热把反应混合物缓慢地倒入盛有250mL冷水的烧杯中,乙酰苯胺晶体析出。充分冷却至室温后,减压过滤,用洗涤晶体2~3次。用滤液冲洗烧杯上残留的晶体,再次过滤,两次过滤得到的固体合并在一起。
Ⅱ.乙酰苯胺的提纯
将上述制得的粗乙酰苯胺固体移入500mL烧杯中,加入100mL热水,加热至沸腾,待粗乙酰苯胺完全溶解后,再补加少量蒸馏水。稍冷后,加入少量活性炭吸附色素等杂质,在搅拌下微沸5min,趁热过滤。待滤液冷却至室温,有晶体析出,称量产品为11.2g。
回答下列问题:
A.乙醇 B.CCl4 C.冷水 D.乙醚
A.升温 B.采用高压氧酸浸 C.使用98%的浓硫酸 D.将矿石粉碎成小块
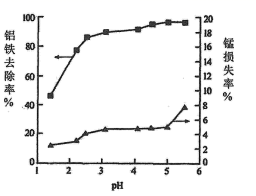
A.1~2 B.2~3 C.3~4 D.4~5
已知在此条件下Mn2+不会产生沉淀,推测锰元素损失的可能原因是。


已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 金属离子 | Fe2+ | Fe3+ | Al3+ | Ni2+ | Co2+ |
| 开始沉淀的pH | 6.3 | 1.5 | 3.4 | 6.2 | 7.15 |
| 沉淀完全的pH | 8.3 | 2.8 | 4.7 | 8.9 | 9.15 |
a铁 b氨水 c碳酸钠溶液 d.稀硫酸

溶液中Ni2+离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Ni2+ |
| 开始沉淀时(c=0.01mol·L-1)的pH | 7.2 |
| 沉淀完全时(c=1.0×10-5mol·L-1)的pH | 8.7 |
回答下列问题:
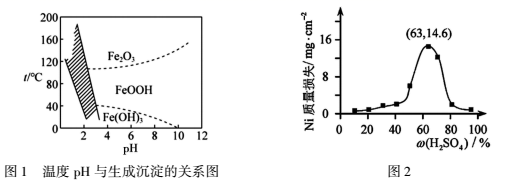
 请回答下列问题:
请回答下列问题:


某校化学兴趣小组根据该流程在实验室中进行实验。回答下列问题:

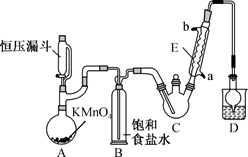
①装置A中盛装浓氨水的仪器名称为 ;橡皮管a的作用是。
②装置B中加入CCl4的目的是。
③装置D中发生的离子方程式是。
④装置C中的试剂b是。

|
序号 |
l |
2 |
3 |
4 |
|
标准溶液体积/ mL |
20.05 |
18.40 |
19.95 |
20.00 |
所得产品硫酸氢钠的纯度为(以百分数表示,保留三位有效数字)。

有关物质的部分性质如表:
| 物质 | 熔点/℃ | 沸点/℃ | 其他性质 |
| PCl3 | -112 | 75.5 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
| POCl3 | 2 | 105.3 | 遇水生成H3PO4和HCl,能溶于PCl3 |
请按要求回答下列问题:
Ⅰ.取m克产品于锥形瓶中,加入足量NaOH溶液,待完全反应后加入足量试剂M;
Ⅱ.向锥形瓶中加入0.1000mol·L-1的AgNO3溶液50.00mL,使Cl-完全沉淀;
Ⅲ.向其中加入2mL硝基苯,用力摇动,使沉淀表面被有机物覆盖:
Ⅳ.加入指示剂,用cmol·L-1NH4SCN溶液滴定过量Ag+至终点,记下所用体积为VmL。
已知:Ksp(AgCl)=3.2×10-10 , Ksp(AgSCN)=2×10-12
①试剂M为。
②Cl元素的质量分数=(列出算式)。
③若取消步骤Ⅱ,会使步骤Ⅳ中将出现两种沉淀共存,此时c(Cl-):c(SCN-)=。这样操作会造成结果(填“偏大”或“偏小”或“无影响”)。
已知:①常温下ClO2为黄绿色气体,其熔点为-59℃,沸点为11.0℃,能溶于水,不与水反应。②温度过高,ClO2的水溶液可能爆炸。
实验室利用如图所示装置模拟工业NaClO3与Na2SO3在浓H2SO4存在下制备ClO2 , 并以ClO2为原料制备NaClO2(已知:高于60℃时,NaClO2分解生成NaClO3和NaCl)。

步骤1:准确量取ClO2溶液20.00 mL,稀释成100.0 mL试样;量取V1 mL试样加入到锥形瓶中;
步骤2:调节试样的pH≤2.0加入足量的KI晶体,振荡后,静置片刻;
步骤3:加入指示剂X,用a mol/L的Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。
已知:2ClO2+8H++10I-=5I2+2Cl-+4H2O I2+2Na2S2O3=2NaI+Na2S4O6
①步骤I中量取20.00 mL ClO2溶液所用的仪器为(选填“酸式"或“碱式”)滴定管。
②指示剂x为,滴定终点的实验现象是。原ClO2溶液的浓度为g/L(用含字母的代数式表示)。

已知:铍及其化合物具有与铝及其化合物相似的化学性质。回答下列问题:
 已知:i.叠氮化钠受热或剧烈撞击易分解,具有较强的还原性。
已知:i.叠氮化钠受热或剧烈撞击易分解,具有较强的还原性。
ii.相关物质的物理性质如下表:
| 相关物质 | 熔点℃ | 沸点℃ | 溶解性 |
| CH3OH | -97 | 67.1 | 与水互溶 |
| 亚硝酸甲酯(CH3ONO) | -17 | -12 | 溶于乙醇、乙醚 |
| 水合肼(N2H4·H2O) | -40 | 118.5 | 与水、醇互溶,不溶于乙醚和氯仿 |
| NaN3 | 275 | 300 | 与水互溶,微溶于乙醇,不溶于乙醚 |

①步骤II三颈烧瓶中发生反应的化学方程式为。该反应放热,但在20℃左右选择性和转化率最高,实验中控制温度除使用冷水浴,还需采取的措施是。
②步骤II开始时的操作为(选填字母编号)。步骤III蒸馏时的操作顺序是(选填字母编号)。
a.打开K1、K2 b.关闭K1、K2 c.打开K3 d.关闭K3 e.水浴加热 f.通冷凝水
2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑
Ce4++Fe2+=Ce3++Fe3+
称取2.50 g产品配成250 mL溶液,取25.00 mL置于锥形瓶中,加入V1 mLc1 mol·L-1(NH4)2Ce(NO3)6溶液,充分反应后稍作稀释,向溶液中加适量硫酸,滴加2滴邻菲哕啉指示剂,用c2 mol·L-1(NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+ , 消耗标准溶液V2 mL。
①产品纯度为。
②为了提高实验的精确度,该实验还需要。

已知:①“酸浸”时V2O5和V2O4先与稀硫酸反应分别生成VO 和VO2+。
②有机萃取剂萃取VO2+的能力比萃取VO 的能力强。
③溶液中VO 与VO
可相互转化:VO
+H2O
VO
+2H+。
①“沉钒”时,钒元素主要以形式存在(填相应的离子符号)。
②实验发现,温度超过80℃以后沉钒率下降(如图),可能的原因是。
