① 实验A中水的作用是,
② 实验B中的水隔绝了烧杯中白磷与空气的接触,还起到了作用。

① 通电后电极上出现气泡,a试管中产生的气体是。
② 电解水时加少量Na2SO4的目的是。
③ 由此实验得出结论:水是由元素组成的。

资料: Na2SO4溶液呈中性,其中含有浓度极低的 H+和 OH-。
步骤1:向装置中重新装满含少量Na2SO4的水,接通电源,一段时间后关闭电源。
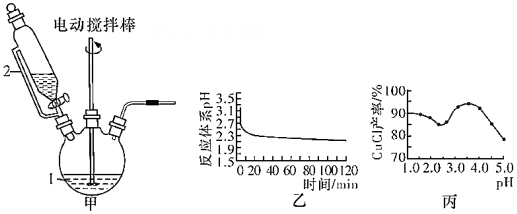
步骤2:分别取出管a和管b电极附近的溶液,并测定溶液的pH。经测定:管a中溶液pH小于7,管b中溶液pH大于7。
①图中能表示电解时管a中水在电极端所发生变化的结果的是。
② 当电解水实验结束,倒出装置中的溶液测定其pH,则pH7(填写“<”、“>”或“=”)
乙醇汽油是将燃料乙醇(C2H5OH)以一定比例添加到汽油中形成的新型替代能源。燃料乙醇的来源可分为生物来源与非生物来源两大类。生物燃料乙醇主要有以下几种分类: ①富含淀粉(糖类),以玉米、小麦等粮食作物为原料的粮食乙醇(称为“I代”); ②富含纤维素,以玉米芯、玉米秸秆等纤维素物质为原料的农作物秸秆乙醇(称为“Ⅱ代”); ③以木薯、甜高粱茎秆等经济作物为原料的第1.5代非粮食乙醇。生物燃料乙醇不含硫,无灰分,且具有良好的环保性……同时,生物燃料乙醇还具有可再生性。国标乙醇汽油E10是用90%的普通汽油与10%的燃料乙醇调和而成的。根据交通部汽车运输行业能源利用监测中心的测试结果显示,使用E10乙醇汽油后,排放的尾气中一氧化碳减少了19.7%,碳氢化合物减少了16.4%。在当前化石能源资源日益短缺、石油安全形势日益严峻和全球碳减排压力不断加大的背景下,生物燃料乙醇已经被视为替代和节约汽油的最佳燃料。





① 工业可以利用NaOH溶液实现二氧化碳的捕集,写出该原理的化学反应方程式
② 二氧化碳是一种重要的资源
a.在高温高压下,CO2和NH3可以合成尿素[CO(NH2)2],同时生成水,该反应中参加反应的CO2与NH3的分子个数比是。
b.一定条件下,CO2和H2反应生成CH4和H2O。
请在右边框图中将该反应的微观粒子补充完整。

粗盐中含有 Na2SO4、MgCl2、CaCl2等可溶性杂质。为进一步除杂,向粗盐水中依次加入四种试剂:BaCl2溶液、NaOH溶液、Na2CO3溶液、稀盐酸(所加试剂均过量),加入稍过量的NaOH溶液作用是(用化学方程式表示,下同),加入稍过量的Na2CO3溶液,除了能除尽粗盐中的CaCl2外,它还有一个作用是。


① 步骤1中分子的发生了变化。
A.间距 B.质量 C.种类 D.个数
② 溶液a、b、c中属于氯化钠饱和溶液的是
③ 溶液b的质量(选填“<”、“=”或“>”)溶液c的质量。
下列操作会导致配得的NaCl溶液溶质质量分数偏小的是____。

① 写出电解槽中发生反应的化学方程式:,该反应前
后元素化合价升高。(填元素名称)
② 检验烧碱样品中是否含有Na2CO3 , 下列试剂中可选择使用的是。
A.酚酞 B.硝酸钾溶液 C.稀盐酸 D.澄清石灰水
③ 氯碱工业生产的烧碱样品中常含有Na2CO3和NaCl等杂质,烧碱样品中氢氧化钠质量分数 98.0%为合格品。称取20.3g样品,加足量水溶解,再加入足量的氯化钡溶液充分反应,过滤得到滤渣和滤液。向滤液中加入几滴酚酞,再逐滴加入稀盐酸至恰好完全反应,共消耗质量分数为5%的稀盐酸365g,请判断该烧碱样品是否为合格品。(不考虑其他杂质参加反应)(写出计算过程)。