钆元素是一种比较活泼的稀土元素。钆有多种同位素(质子数相同而中子数不同的同一元素的不同原子互称为同位素),如钆156、钆157、钆158等。钆157的相对原子质量为157,核电荷数为64,中子数为93。
①钆是一种银白色金属;②钆具有延展性;③钆的熔点为1313℃,沸点为3266℃;④钆在干燥的空气中比较稳定,在潮湿的空气中会形成松散易脱落的片状白色氧化物:⑤轧能与水缓慢反应;⑥钆能与酸形成无色的盐。
在很多领域可以看到钆元素的应用。比如利用金属钆或其合金可以生产一种小型高效磁制冷器,减少氟利昂等冰箱制冷剂的使用;钆的水溶性顺磁络合物在医疗上可提高人体的核磁共振(NMR)成像信号;钆用作控制核电站的连锁反应级别的抑制剂,以保证核反应的安全等。

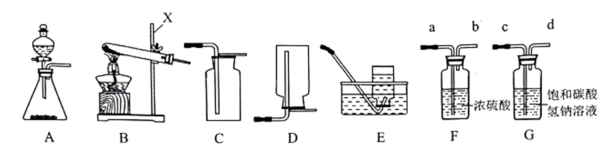
①写出仪器X的名称。
②实验室用大理石和稀盐酸反应制取二氧化碳,应选用的发生装置为(填字母序号),反应的化学方程式为。
③实验室常用加热无水醋酸钠固体的方法来制取甲烷,已知甲烷气体的密度比空气小,且难溶于水,则制取并收集甲烷可以选用的装置组合为(填字母序号)。
实验室制得的二氧化碳气体中常含有少量的氯化氢和水蒸气,为了得到纯净干燥的二氧化碳气体,除杂装置的导管气流方向连接顺序正确的是____(填字母序号)。
某同学用收集的干燥的氧气,探究蜡烛的组成中是否含有碳、氢元素。实验装置如图所示。
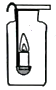
①用集气瓶收集干燥的氧气,应选用(填“向上排空气法”、“向下排空气法”或“排水法”)。
②将蜡烛点燃,伸入集满氧气的集气瓶中,盖上玻璃片。一段时间后取出蜡烛,观察到烧杯内壁有水雾,得到的结论是:蜡烛中含有元素。为继续探究蜡烛的组成中是否含有碳元素,你补充的实验操作为。
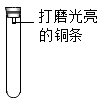
【提出问题】铜生锈与哪些因素有关?
【查阅资料】①铜表面绿色锈渍的化学成分主要是碱式碳酸铜[ Cu2(OH)2CO3]。
②常温下,亚硫酸钠(Na2SO3)可与氧气发生化合反应。
【猜想与假设】常温下,铜生锈可能与氧气、水蒸气、二氧化碳有关。
【进行实验】通过控制与铜条接触的物质,利用上图装置(铜条长度为3cm,试管容积为20mL)分别进行下列4个实验,并持续观察30天。
序号 | 主要实验操作 | 实验现象 |
1 | 加入2mL氢氧化钠浓溶液 | 铜条始终无明显变化 |
2 | 先加入2mL浓硫酸,再通入约4mL二氧化碳 | 铜条始终无明显变化 |
3 | 先加入4mL饱和Na2SO3溶液,再充满二氧化碳 | 铜条始终无明显变化 |
4 | 先加入2mL蒸馏水,再通入约4mL二氧化碳 | 铜条小部分出现绿色锈渍 |
【解释与结论】
在进行猜想与假设时,同学们认为铜生锈与二氧化碳有关,其依据是。
查阅资料:下表是部分物质的溶解性(20℃)。
阴离子阳离子 | Cl- | ||
Na+ | 溶 | 溶 | 溶 |
Ag+ | 不 | 不 | 溶 |
实验操作 | 实验现象 | 实验结论 |
取少量样品于试管中,加水溶解,滴加少量硝酸银溶液。 | 有。 | 样品中有氯化钠 |
有同学提出上述实验方案不正确,请你继续完善上述实验方案(写出具体实验操作、实验现象)。
已知氯化钠、碳酸钠在不同温度时的溶解度如下。
0℃ | 10℃ | 20℃ | 30℃ | 40℃ | |
氯化钠/g | 35.7 | 35.8 | 36 | 36.3 | 36.6 |
碳酸钠/g | 7 | 12.2 | 21.8 | 39.7 | 49.0 |
可以采用(填“蒸发结晶”或“降温结晶”)的方法提纯碳酸钠。
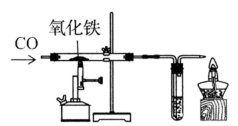
②装置中导管末端加一个点燃的酒精灯的作用为。
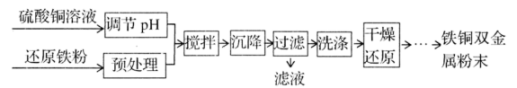
①"搅拌"时发生的化学反应利用了铁的金属活动性比铜的(填“强"或“弱")。
②“过滤"后所得滤液中溶质的主要成分是(填化学式)。
③若用该工艺制备了1000g铁铜双金属粉末产品,其中铜单质的质量分数为12.8%。请你计算置换这些铜单质所需还原铁粉的质量(写出具体的计算过程)。
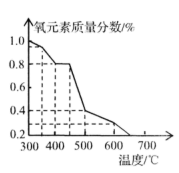
④“干燥还原”可在不同的温度下进行,所得产品中只含有三种元素,其中氧元素的质量分数随温度的变化如下图所示。若③中产品是在500℃时干燥还原后得到的,则其中最多含铁元素。