
溶液 | 加入物质 | 对应的图象 |
⑴饱和石灰水 | 通过量CO2气体 | |
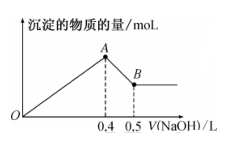
⑵氯化铝溶液 | 加入过量氨水 | |
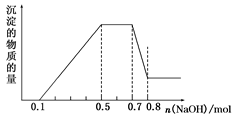
⑶MgCl2、AlCl3的混合液 | 逐滴加入NaOH溶液至过量 | |
⑷含少量NaOH的NaAlO2溶液 | 逐滴加入稀盐酸 |
![]()
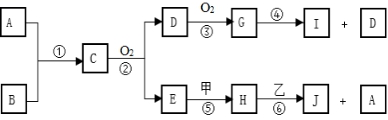
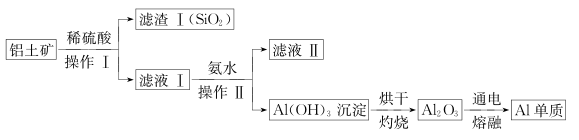 ①Al2O3与稀硫酸反应的离子方程式为 。
①Al2O3与稀硫酸反应的离子方程式为 。
②滤液II中溶质的用途之一是 。
③电解熔融的 Al2O3除得到金属铝之外,还可得到的气体产物是 (填化学式)。工业上在电解熔融的 Al2O3 时,还加入了冰晶石(Na3AlF6)作熔剂,其作用是降低 Al2O3的熔点。冰晶石在物质的分类中属于(填字母)。
a.酸 b.碱 c.盐 d.氧化物