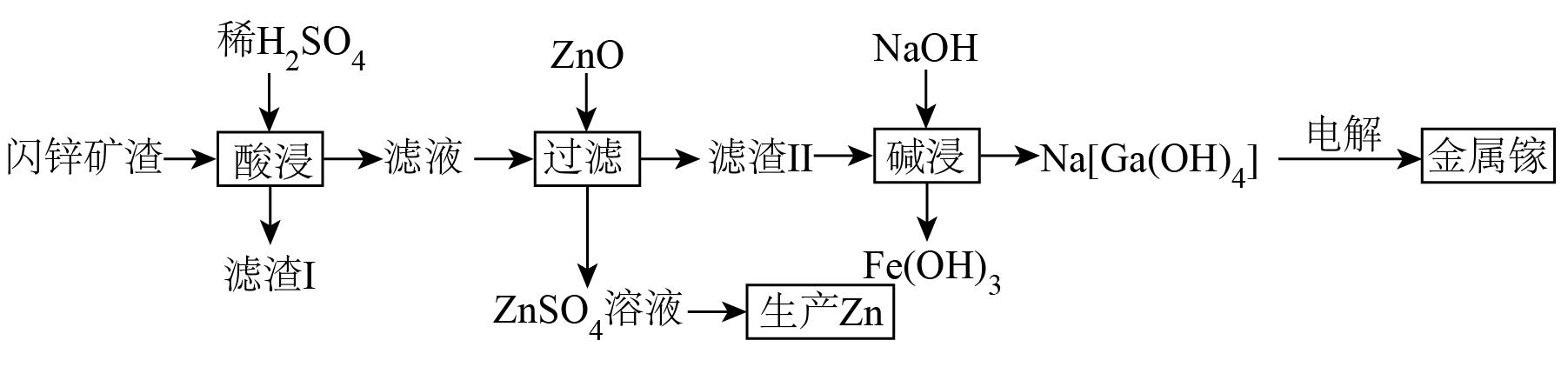
已知:①金属镓在化学性质上非常接近金属铝,其单质、氧化物和氢氧化物均有两性;
②闪锌矿渣通常含有 ,
、
, 硅酸盐等杂质;
③25℃时,、
。
回答下列问题:
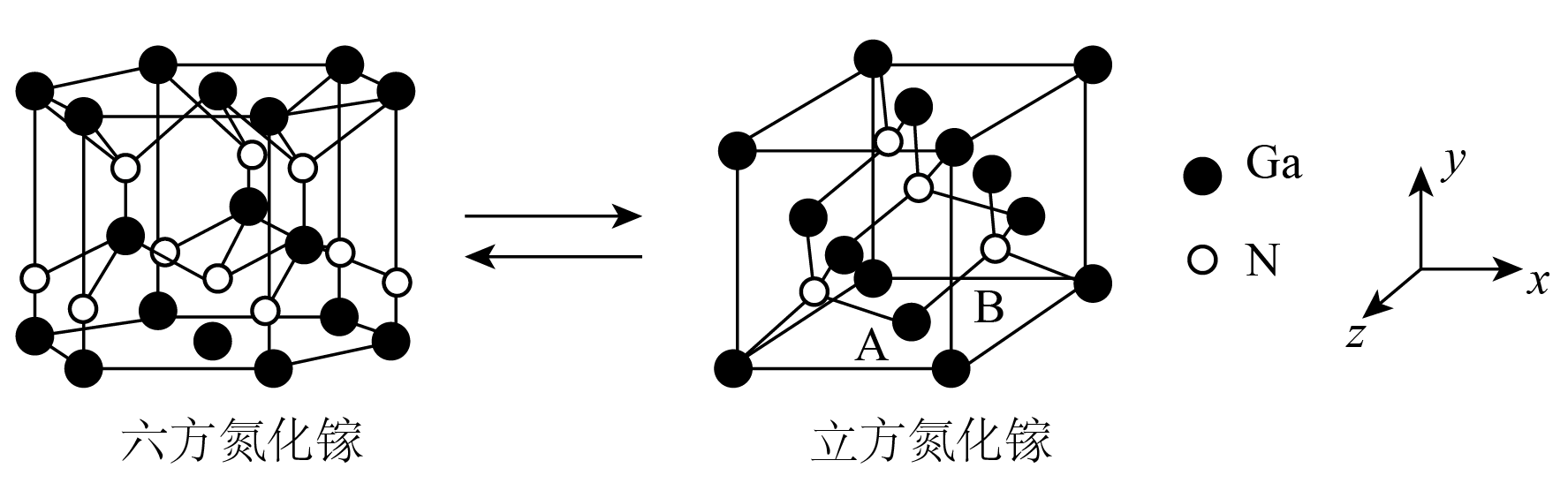
①六方氮化镓晶体硬度极高,熔点为1700℃,其高温熔融物不导电。六方氮化镓属于晶体。
②写出六方氮化镓晶胞的组成:。
②若立方氮化镓的边长为a nm,则其密度为(列出计算式)。
①苯环上有二个取代基:②与FeCl3溶液发生显色反应;
③能发生水解反应,但不能发生银镜反应。
 , 为原料合成
, 为原料合成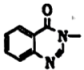 的路线(无机试剂任选)。
的路线(无机试剂任选)。
已知:①主要副反应为
②温度过高会引发烃裂解生成炭(C)。
③相关化学键的键能如下所示:
化学键 | ||||
键能 | 615 | 436 |
请回答:
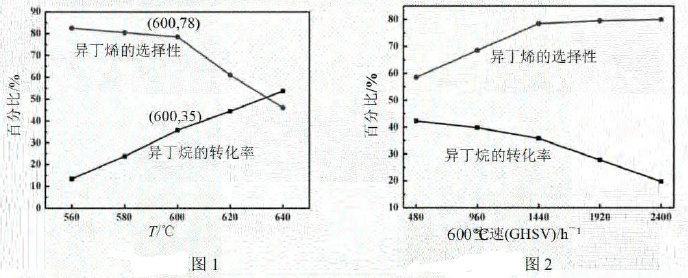
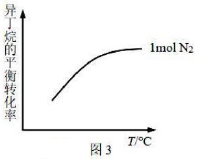
①图1中,600℃时异丁烯收率。
②下列说法正确的是。
A.由图1可知,温度越高,产生异丁烯的速率越快
B.混入的目的之一是减小异丁烷的吸附速率,同时带走催化剂局部多余的热量,从而抑制催化剂的积碳
C.图2中,空速增加,异丁烷转化率降低的原因可能是原料气在催化剂中停留时间过短
D.图2中,空速增加,异丁烯选择性升高的原因可能是原料气将产物迅速带走,抑制了副反应的发生
③图1中,随着温度升高,异丁烷转化率增大而异丁烯选择性下降的原因可能是。
④其他条件相同,异丁烷的平衡转化率如图3所示。若充入改为2mol,在图3中作出异丁烷的平衡转化率随温度变化的曲线(忽略积碳的影响)。