 C . 乙酸甲酯的结构简式:C3H6O2
D . NH3的电子式:
C . 乙酸甲酯的结构简式:C3H6O2
D . NH3的电子式:选项 | 实验探究方案 | 探究目的 |
A | 向盛有Fe(NO3)2溶液的试管中滴加几滴稀硫酸,振荡,观察溶液颜色变化 |
|
B | 向溶液X中加入稀硫酸,并将产生的无色气体通入澄清石灰水中,观察是否有沉淀生成 | 溶液X中含有 |
C | 用pH试纸分别测定浓度均为0.1mol/L的NaCN和NaClO溶液的pH | |
D | 常温下,向10mL0.1mol/LNaCl溶液中滴加5滴0.1mol/LAgNO3溶液,充分反应后,再滴加5滴0.1mol/LKI溶液,观察沉淀颜色变化 |

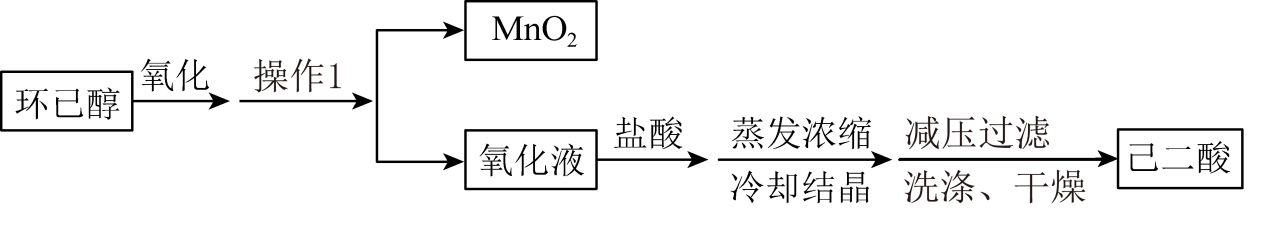
已知:“氧化”过程发生的主要反应为:![]()
KOOC(CH2)4 COOK △H<0
该反应装置如图所示。
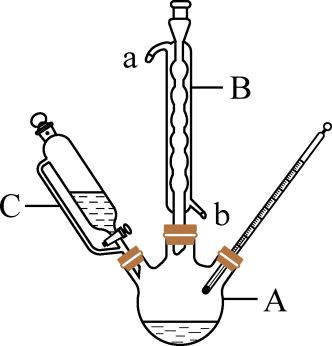
回答下列问题:

物质 | 己二酸 | 氯化钠 | 氯化钾 |
25℃时溶解度/g | 2.1 | 36.1 | 34.3 |
70℃时溶解度/g | 68 | 37.8 | 48 |
100℃时溶解度/g | 160 | 39.5 | 56.3 |
①己二酸晶体“洗涤”的方法为(填字母)。
A.用乙醇洗涤 B.用热水洗涤 C.用冷水洗涤
②除去己二酸晶体中含有的氯化钠杂质通常采取的实验方法为。
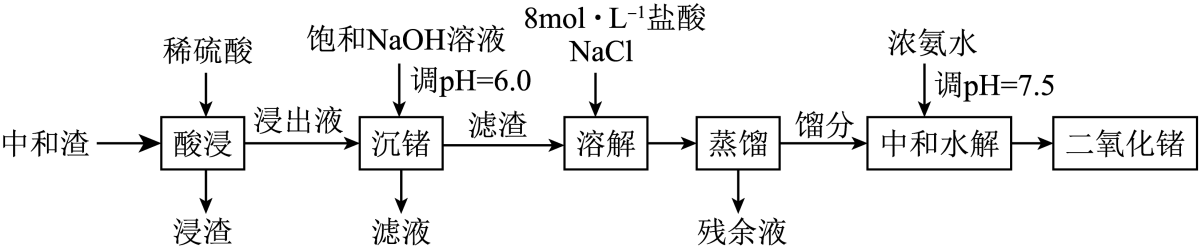
已知:
①GeCl4的沸点:83℃,FeCl3的沸点:315℃。
②H2GeO3在高酸度时易聚合形成胶状多聚锗酸。
③常温下,部分金属阳离子转化为氢氧化物沉淀的pH见下表(离子浓度低于10-5 mol·L-1视为沉淀完全)。
离子 | Fe3+ | Zn2+ |
开始沉淀pH | 2.2 | 6.2 |
完全沉淀pH | 3.2 | 8.2 |
回答下列问题:
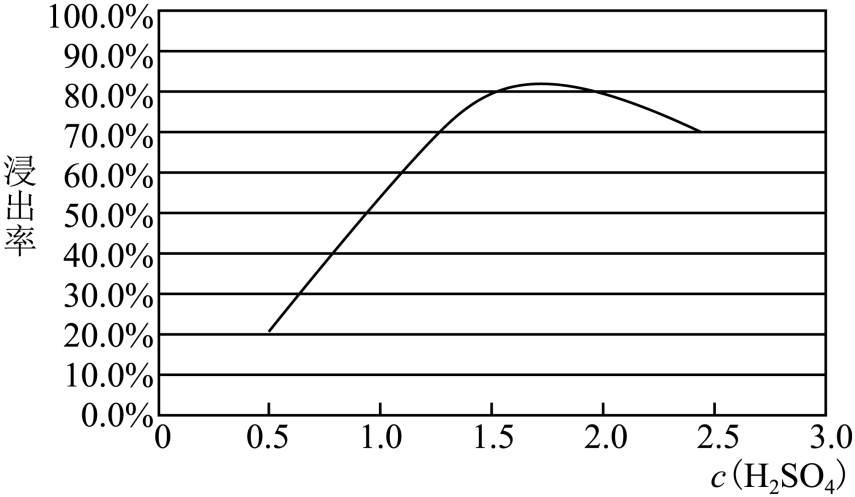
②测得相同时间内锗的浸出率与硫酸的物质的量浓度(mol·L-1)的关系如图所示。硫酸浓度过高,浸出率反而降低的原因是。
称取m g GeO2样品,在加热条件下溶解,用NaH2PO2将其还原为Ge2+ , 用c mol·L-1 KIO3标准溶液滴定,消耗KIO3标准溶液的平均体积为V mL,需选用的指示剂为,样品纯度为%。(实验条件下,NaH2PO2未被KIO3氧化)[已知:+H+
Ge4++I-+H2O(未配平);
]。
①CO2(g) +3H2(g) ⇌ CH3OH(g)+ H2O(g) ΔH1
②CO2(g)+ H2(g) ⇌CO(g)+H2O(g) ΔH2=+41.2kJ·mol-1
已知:CO(g)+2H2(g) ⇌ CH3OH(g) ΔH = -90.6kJ·mol-1 , 则△H1= 。
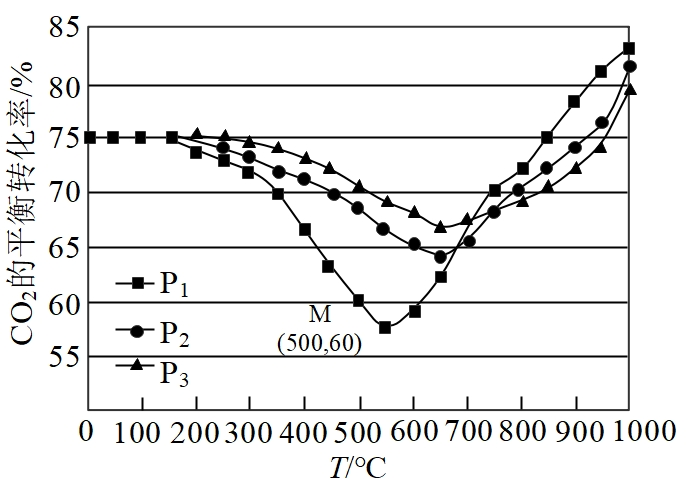
①压强p1、p2、p3由大到小的顺序是。压强为p1 时,温度高于570 ℃之后,随着温度升高CO2平衡转化率增大的原因是。
②图中点M(500,60),此时压强p1为0.1 MPa,CH3OH的选择性为(选择性:转化的CO2中生成CH3OH占整个转化的CO2的百分比)。则该温度时反应①的平衡常数Kp=(MPa)-2(分压=总压×物质的量分数)。
在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图所示:

阴极电极反应为,该装置中使用的是(填“阴”或“阳”)离子交换膜。
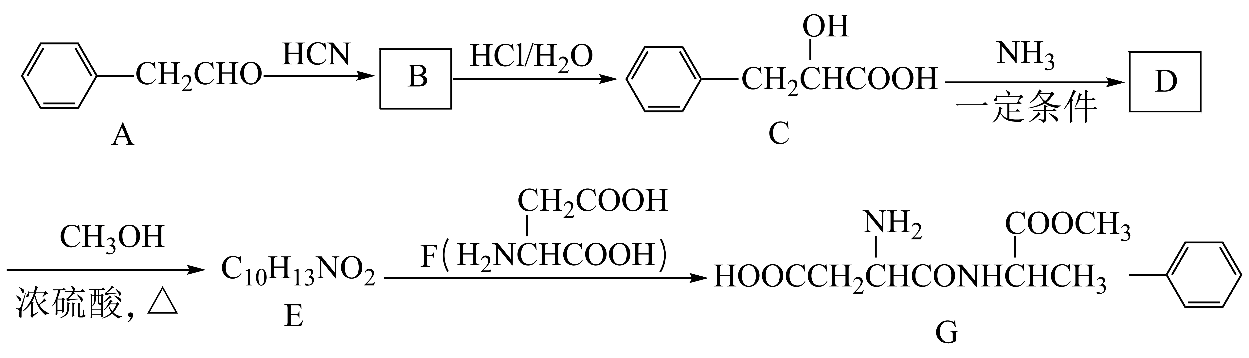
已知如下信息:
①![]()
![]()
②![]()
![]()
回答下列问题:
①分子中含有苯环,且苯环上有两个取代基
②能与FeCl3溶液发生显色反应
③能在氢氧化钠溶液中发生水解反应,且含有苯环的水解产物的核磁共振氢谱只有一组峰