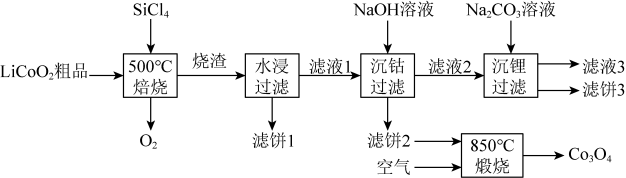
回答下列问题:
a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
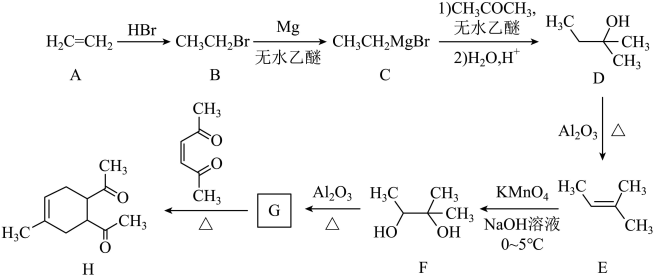
回答下列问题:
 ,H在碱性溶液中易发生分子内缩合从而构建双环结构,主要产物为I(
,H在碱性溶液中易发生分子内缩合从而构建双环结构,主要产物为I( )和另一种α,β-不饱和酮J,J的结构简式为。若经此路线由H合成I,存在的问题有(填标号)。
)和另一种α,β-不饱和酮J,J的结构简式为。若经此路线由H合成I,存在的问题有(填标号)。 a.原子利用率低 b.产物难以分离 c.反应条件苛刻 d.严重污染环境


实验②中Cu溶解的离子方程式为;产生的气体为。比较实验①和②,从氧化还原角度说明的作用是。
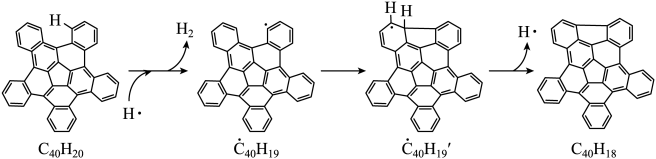
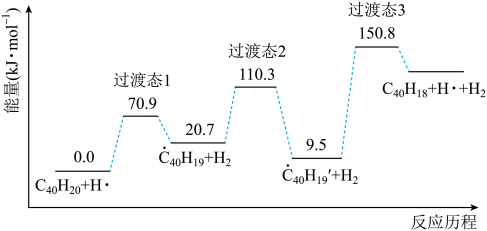
回答下列问题:

a.升高温度 b.增大压强 c.加入催化剂