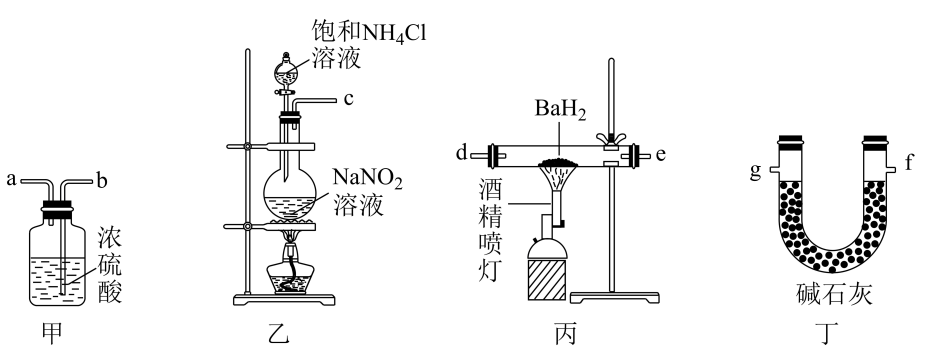

实验操作 | 实验现象 | 实验结论 | |
A | 把 | 有白色沉淀产生 | X气体具有强氧化性 |
B | 葡萄糖溶液中加入新制氢氧化铜悬浊液 | 有砖红色沉淀生成 | 葡萄糖具有还原性 |
C | 向鸡蛋清溶液中滴入几滴硫酸铜溶液 | 产生白色沉淀,加水后沉淀不溶解 | 蛋白质发生了变性 |
D | 向某溶液中加入稀硫酸 | 生成淡黄色沉淀和刺激性气味气体 | 该溶液中一定含有 |

实验 | 结论 | |
A | 将乙烯通入溴的四氯化碳溶液,溶液最终变为无色透明 | 生成的1,2-二溴乙烷无色、可溶于四氯化碳 |
B | 乙醇和水都可与金属钠反应产生可燃性气体 | 乙醇分子中的氢与水分子中的氢具有相同的活性 |
C | 用乙酸浸泡水壶中的水垢,可将其清除 | 乙酸的酸性大于碳酸的酸性 |
D | 甲烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红 | 生成的氯甲烷具有酸性 |
用K2CO3溶液吸收H2S。
已知:氢硫酸和碳酸的电离常数如下表。
|
| | |
| H2S | 1.1×10-7 | 1.3×10-13 |
| H2CO3 | 4.5×10-7 | 4.7×10-11 |
①用化学用语表示K2CO3溶液显碱性的原因:。
②用过量的K2CO3溶液吸收H2S的离子方程式是。
在密闭容器中发生反应。其他条件不变时,H2S的平衡转化率随温度和压强的变化如下图。

①P3>P2>P1 , 反应中S2(填“是”或“不是”)气态,理由是。
②实际反应在高温下进行的原因是。
间接电解法脱硫过程的示意图如下。

①溶液X的主要溶质是。
②简述在电解反应器中FeCl3溶液再生的原理:。
③不考虑其他副反应,理论上5 mol H2S反应能生成gH2。
Ⅰ.用间接碘量法标定硫代硫酸钠溶液的浓度:用分析天平准确称取基准物质K2Cr2O7(摩尔质量为294g·mol-1)0.5880g。平均分成3份分别放入3个锥形瓶中,加入水均配成20.00mL溶液,加入过量的KI并酸化,发生反应:6I-+Cr2O+14H+=3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用Na2S2O3溶液滴定,发生反应:I2+2S2O
=2I-+S4O
, 三次消耗Na2S2O3溶液的平均体积为20.00mL。
实验编号 | 反应温度/℃ | 0.1mol·L-1稀硫酸的体积/mL | 0.1mol·L-1硫代硫酸钠溶液的体积/mL | 加入的水的体积/mL | 产生等量的沉淀所需时间/s |
① | 20 | 2 | 1 | V1 | t1 |
② | 30 | 2 | 1 | 2 | t2 |
③ | 30 | 2 | V2 | 1 | t3 |
实验(填实验编号)是探究硫代硫酸钠溶液的温度对反应速率的影响。

回答下列问题:
a.溶解和乙烯 b.作催化剂 c.促进气体反应物间的接触
室温下进行如下两组实验,实验数据如表所示:
实验编号 | ① | ② |
实验试剂 | | |
酸性 | 116 | 6 |
试管①中溶液褪色的速率开始十分缓慢,一段时间后突然加快。
为配制的草酸溶液,所需要的实验仪器主要有天平(含砝码)、量筒、烧杯、药匙、、和。
小组同学设计如下三组实验,通过测定褪色所需时间来判断反应的快慢。
实验编号 | | 酸性 | 温度/ | ||
浓度 | 体积 | 浓度 | 体积 | 25 | |
③ | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
④ | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
⑤ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
探究温度对化学反应速率影响的实验编号是(填编号,下同),探究反应物浓度对化学反应速率影响的实验编号是。


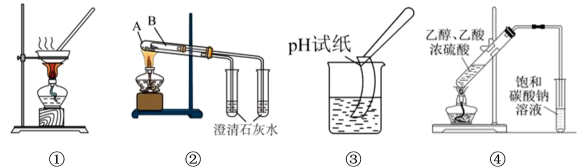
实验结束后,烧杯D中上层出现透明的、不溶于水的油状液体。
①在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入几块碎瓷片,其目的是。
②仪器C的名称是。在该实验中,它的作用除了冷凝,还可以。
③烧杯D中盛放的溶液是,它的作用是(填字母)
a.中和乙酸和乙醇
b.中和乙酸,吸收乙醇
c.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,利于它分层析出
d.加速酯的生成,提高其产率
④在实验室制备乙酸乙酯的实验中,要制备1 mol乙酸乙酯所需的B和D远大于1 mol(不考虑原料的挥发损耗),原因是。
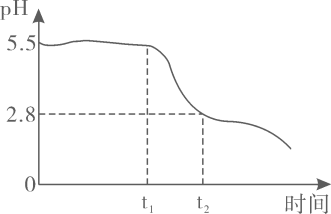
已知:①当时,
开始溶解。
②相关离子生成氢氧化物沉淀的如下表
离子 | 开始沉淀的 | 沉淀完全的 |
| 2.7 | 3.7 |
| 5.7 | 9.0 |


若用乙醇和
在浓硫酸作用下加热,充分反应,能否(填“能”或“不能”)生成
, 其原因是
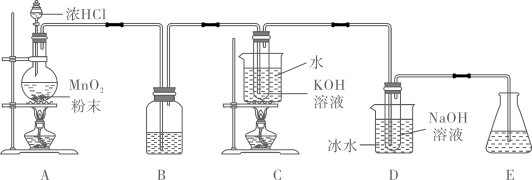
回答下列问题:

操作:向1号和2号试管中,滴加中性KI溶液。
现象:1号试管溶液颜色不变,2号试管溶液变为棕色。
结论:该条件下氧化能力NaClO。(填“大于”或“小于”)

已知:①熔砂为对应金属元素的含氧酸盐(、
等)
② ,
;
③的溶解度(
水):0.48(20℃)、1.32(40℃)、2.42(60℃)


①滤渣A煅烧得到Al2O3 , 再用电解法冶炼Al。冶炼Al的化学方程式是。
②滤渣B受热分解所得物质可以循环利用,B是。
③已知:
滤液3中的浓度是0.04 mol/L,则
的浓度是mol/L。
不同温度下化合物的溶解度(g/100gH2O)
|
化合物名称 |
0℃ |
20℃ |
40℃ |
60℃ |
80℃ |
|
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
|
KCl |
28.0 |
34.2 |
40.1 |
45.8 |
51.3 |
|
K2SO4 |
7.4 |
11.1 |
14.8 |
18.2 |
21.4 |
|
K2Cr2O7 |
4.7 |
12.3 |
26.3 |
45.6 |
73.0 |
|
Na2Cr2O7 |
163 |
183 |
215 |
269 |
376 |
结合表中数据分析,过程Ⅱ得到K2Cr2O7粗品的操作是:,过滤得到K2Cr2O7粗品。