(提出问题)该淡黄色固体的化学成分是什么?
(查阅资料)
Ⅰ.硫单质是一种淡黄色固体,难溶于水,在空气中点燃硫单质,生成一种无色、有刺激性气味的气体。
Ⅱ.过氧化钠(Na2O2)是一种淡黄色固体,能与水反应,生成气体并放出大量的热。
(设计实验方案)
方案一:取少量该固体粉末于试管中,加2mL水,振荡并观察现象。
方案二:在燃烧匙里放少量该固体,在酒精灯上加热,观察现象。
小明向盛有少量该固体的试管中加入2mL水,立刻观察到有无色气泡产生,并且验证出该反应同时生成了氢氧化钠(NaOH),确定该淡黄色粉末为过氧化钠(Na2O2)。
小明还想对生成的气体成分进行判断,他提出了以下三种假设:
A.该气体是CO2 B.该气体是O2 C.该气体是H2
同学们首先一致认为上述假设中的(填“A”或“B”或“C”)肯定不合理,理由是。
通过查阅资料,同学们又得知:在化学反应中,有元素化合价升高,就必然有元素化合价降低。于是通过小组讨论,大家一致认为上述假设中B成立。同学们用图1装置(装置气密性良好)进行实验检验,验证了上述分析的合理性:
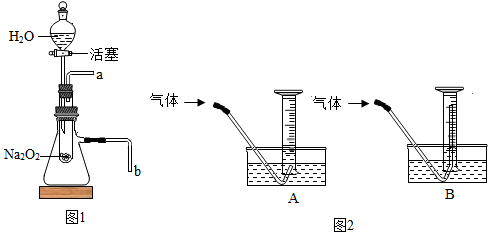
下列关于Na2O2说法错误的是___________(填字母)。
进一步查阅资料可知:在潜水艇中常用过氧化钠(Na2O2)来吸收艇上人员呼出的二氧化碳,同时生成碳酸钠和供人们呼吸的气体,写出该反应的化学方程式。