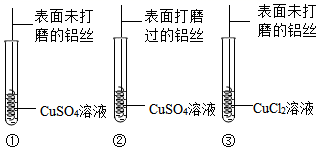
(讨论交流)金属铝在常温下易与空气中的氧气反应生成致密的氧化铝薄膜。实验③中的铝丝表面会析出红色固体,是因为CuCl2溶液中的粒子破坏了铝表面的氧化铝薄膜,是哪种粒子破坏了铝表面的氧化铝薄膜呢?
(猜想与假设)猜想I:H2O;
猜想Ⅱ:Cu2+;
猜想Ⅲ:。
|
序号 |
实验 |
现象 |
推论 |
|
④ |
向试管④中加入水 |
无明显现象 |
H2O不能破坏氧化铝薄膜 |
|
⑤ |
向试管⑤中加入KCl固体 |
铝表面析出红色固体 |
K+或Cl-能破坏氧化铝薄膜 |
|
⑥ |
向试管⑥中加入K2SO4固体 |
|
K+和SO42-都不能破坏氧化铝薄膜 |
(实验结论)猜想Ⅲ正确。
同学们认为实验④没有必要进行,原因是。
通过对比实验(选填“①”“②”或“③”)可得知,打磨能破坏氧化铝薄膜。
将表面未打磨的铝丝浸入稀硫酸中,整个过程中观察到现象是。
相同条件下,稀盐酸与稀硫酸分别与表面未打磨的铝丝反应,反应速率不同的原因是。