 B .
B . 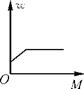 C .
C . 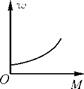 D .
D . 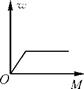




| 物质名称 | 氯化钠 | 氢氧化钙 | 氯酸钾 | 硝酸钾 |
| 溶解度(克/100克水) | 36.0 | 0.165 | 7.4 | 31.6 |

实 验 | ① | ② | ③ | ④ |
水的质量/g | 50 | 50 | 50 | 50 |
加入氯化钠的质量/g | 15 | 20 | 25 | 30 |
未溶解氯化钠的质量/g | 0 | 2 | 7 | 12 |
 B . 溶质质量的变化
B . 溶质质量的变化  C . 溶质的质量分数变化
C . 溶质的质量分数变化 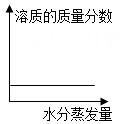 D . 溶液质量变化
D . 溶液质量变化 








实验组别 | 实验1 | 实验2 | 实验3 | ||||
装置甲 | 装置乙 | 装置甲 | 装置乙 | 装置甲 | 装置乙 | ||
电子天平读数(克) | 开始时 | 7.5 | 7.5 | 7.6 | 7.6 | 7.4 | 7.4 |
5分钟后 | 7.1 | 6.5 | 7.3 | 6.7 | 7.0 | 6.6 | |
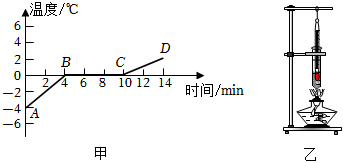
①数据分析:在每组实验中,5 分钟后装置甲的质量都比装置乙大,可以得出装置甲的无纺布中水蒸发得( “快”或“慢”)。
②甲乙装置对照可得出实验结论。

| 实验序号 | 水的质量(g) | 加入氯化钠的质量(g) | 溶液的质量(g) |
| ① | 20 | 4 | 24 |
| ② | 20 | 6 | 26 |
| ③ | 20 | 8 | 27.2 |
| ④ | 20 | 10 | m |
1000g 溶质质量分数80% |
强腐蚀性,阴冷,密封储藏 |
