
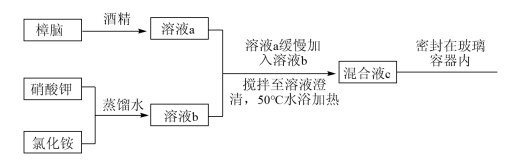
已知:Ⅰ.乙醇、硝酸钾、氯化铵、樟脑之间不相互反应;Ⅱ.樟脑是一种微溶于水的白色固体,化学式为C10H16O。
①樟脑(填“属于”或“不属于”)有机物,其中元素的质量分数最大。
②樟脑(填“易溶”或“难溶”)于酒精。
气温 大气 压强 | 0℃ | 20℃ | 40℃ |
101.3kPa |
|
|
|
100.5kPa |
|
|
|
99.7kPa |
|
|
|
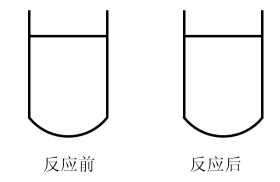
请判断该“天气瓶”能否准确显示天气变化并说明理由。
物质 | 硫酸亚铊(Tl2SO4) | 氢氧化亚铊(TlOH) | 氧化亚铊(Tl2O) | 氯化亚铊(TlCl) |
颜色 | 溶液呈无色 | 溶液呈黄色 | 黑色固体 | 白色固体 |
溶解性 | 易溶 | 易溶 | —— | 难溶 |
发生装置 | 制取的气体 | 所用药品 | 反应的化学方程式 |
| 氧气 | (纯净物) | |
| 氢气 | 锌粒、稀硫酸 |
相同条件下,该小组用石灰石和稀盐酸制CO2 , 并分别用排水法、排食盐水法收集,待收集100mL CO2后,移出导管,每隔一段时间观察并记录量筒内CO2体积。重复实验,所测数据平均值如下表:
时间/h | 0 | 0.5 | 6 | 12 | 24 | 48 |
排水法时CO2体积/mL | 100 | 98.5 | 85.5 | 77 | 66 | 59 |
排食盐水法时CO2体积/mL | 100 | 99 | 93 | 90.5 | 89 | 88 |
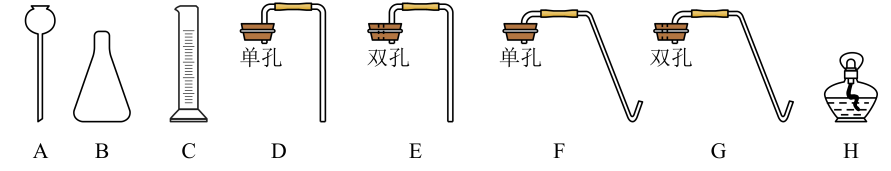
①仪器B的名称是。
②从上图仪器组装完成该探究的实验装置,需要用到(填字母)。
③相同条件下,等体积(填“水”或“食盐水”)吸收CO2更多。
④小组成员通过探究发现,虽然CO2可溶于水,但实验室制取CO2时,也能用排水法收集,理由是。

①通过图像可知自制暖足贴有两点不足,分别是、。
②小组同学猜想两种暖足贴发热情况存在差异的原因,除了受暖足贴各成分的质量及其配比影响外,还可能与蛭石的性质有关。据此猜想蛭石有的特性。
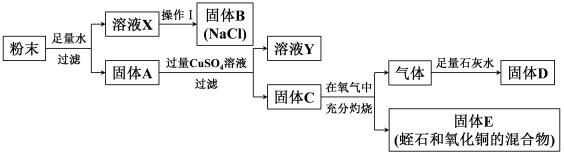
①操作Ⅰ的名称是。
②溶液Y的溶质(填化学式),固体D是(填化学式)。
③根据上述方案,确定蛭石质量最少需要的称量的固体质量有(从固体A~E中选择)。
如图所示,记录所称质量为m1 , 再将铁钉浸入到硫酸铜溶液中,一段时间后记录所称质量为m2。

①可通过观察溶液颜色变为,说明实验过程发生了化学变化。
②测得m1=m2 , 说明参加反应的铁和硫酸铜质量总和等于。

①甲瓶气压数据对应图像中的曲线(填“①”或“②”)。
②反应完全后,向乙瓶继续加入H2O2溶液并观察现象,此实验目的是证明CuSO4。
③再待反应完全后,向乙瓶加入足量的溶液,产生白色沉淀,过滤、洗涤、干燥,称量沉淀物质量为g,证明CuSO4在反应前后质量不变。

①650℃时,CuSO4开始发生分解反应,生成CuO和另一种氧化物X,X的化学式为。
②1000℃时,CuO开始发生分解反应,生成Cu2O和一种单质,计算图中m的值为。