
| 试管编号 | 1 | 2 | 3 | 4 |
| 滴加NaOH溶液的量 | 2滴 | 6滴 | 12滴 | 16滴 |
| 立即观察沉淀的颜色 | 浅绿色 | 浅绿色 | 蓝色 | 蓝色 |
| 酒精灯加热浊液后沉淀的颜色 | 浅绿色 | 浅绿色 | 黑色 | 黑色 |
取浅绿色沉淀用蒸馏水反复洗涤,加入稀盐酸完全溶解,再加入适量BaCl2溶液,产生大量白色沉淀。取蓝色沉淀重复上述实验,无白色沉淀。经检验,试管3、4中黑色沉淀中含有CuO。
下列说法错误的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 蘸有浓氨水的玻璃棒靠近溶液X | 有白烟产生 | 溶液X一定是浓盐酸 |
| B | 用玻璃棒蘸取溶液Y进行焰色反应实验 | 火焰呈黄色 | 溶液Y中一定含Na+ |
| C | 向Fe(NO3)2溶液中滴加硫酸酸化的H2O2溶液 | 溶液变黄 | 氧化性:H2O2>Fe3+ |
| D | 用煮沸过的蒸馏水将Na2SO3固体样品溶解,加稀盐酸酸化,再加入氯化钡溶液 | 有白色沉淀产生 | Na2SO3样品中含有SO42- |
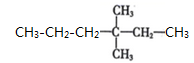
A | B | C | D |
|
|
|
|
验证 | 氨气的收集 | 氯气的净化 | 分离 |

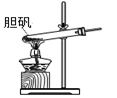 可用于胆矾分解
B .
可用于胆矾分解
B .  可用于检验产物是否含H2O
C .
可用于检验产物是否含H2O
C .  可用于收集SO2
D .
可用于收集SO2
D . 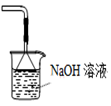 可用于吸收胆矾分解的SO2
可用于吸收胆矾分解的SO2
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | Fe3+具有氧化性 | 用KSCN溶液可以鉴别Fe3+ |
B | 浓硫酸具有脱水性和强氧化性 | 浓硫酸滴到湿润的蔗糖中,蔗糖变成黑色海绵状 |
C | SiO2有导电性 | SiO2可用于制备光导纤维 |
D | 饱和BaSO4溶液中加入饱和Na2CO3溶液有白色沉淀 | Ksp(BaSO4)<Ksp(BaCO3) |
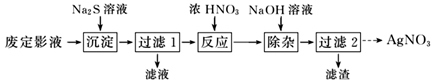
“沉淀”步骤中生成 Ag2S 沉淀,检验沉淀完全的操作是。
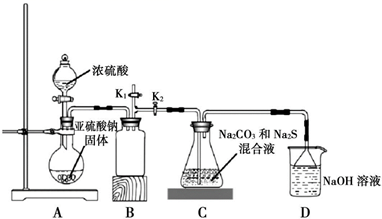
依据图示回答下列问题:
装置 A 中盛放亚硫酸钠固体的玻璃仪器名称是,装置 B 的作用是。

已知:H2SO3、HSO3−、SO32−在水溶液中的物质的量分数随pH的分布如图2,Na2SO3·7H2O和Na2SO3的溶解度曲线如图3。

①为提高NaHSO3的产率,应控制吸收塔中的pH为。
②已知下列反应:
SO2(g)+2OH−(aq)=SO32−(aq)+H2O(l)ΔH1=−164.3kJ·mol−1
CO2(g)+2OH−(aq)=CO32−(aq)+H2O(l)ΔH2=−109.4kJ·mol−1
2HSO3−(aq)=SO32−(aq)+SO2(g)+H2O(l)ΔH3=+34.0kJ·mol−1
吸收塔中Na2CO3溶液吸收SO2生成HSO3−的热化学方程式是。
③吸收塔中的温度不宜过高,可能的原因是(写出1种即可)。
①中和塔中反应的离子方程式为。
②从中和塔得到的Na2SO3溶液中要获得无水Na2SO3固体,需控制温度,同时还要,以防止Na2SO3氧化。
|
实验 |
试剂 |
现象 |
|
|
滴管 |
试管 |
||
|
2 mL | 0.2 mol·L−1 Na2SO3溶液 | 饱和Ag2SO4溶液 | Ⅰ.产生白色沉淀 |
| 0.2 mol·L−1 CuSO4溶液 | Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀 | ||
| 0.1 mol·L−1 Al2(SO4) 3溶液 | Ⅲ.开始无明显变化,继续滴加产生白色沉淀 | ||
已知:Cu+ Cu +Cu2+ , Cu2+
CuI↓(白色) +I2。
①用稀硫酸证实沉淀中含有Cu+的实验现象是。
②通过下列实验证实,沉淀中含有Cu2+和SO32−。

a.白色沉淀A是BaSO4 , 试剂1是。
b.证实沉淀中含有Cu2+和SO32−的理由是。
①推测沉淀中含有亚硫酸根和。
②对于沉淀中亚硫酸根的存在形式提出两种假设:
i.被Al(OH) 3所吸附;
ii.存在于铝的碱式盐中。
对假设ii设计了对比实验,证实了假设ii成立。
a.将对比实验方案补充完整。

步骤二:(按上图形式呈现) 。
任务I:从以下试剂中选择合适的试剂实现→
的转化。
试剂清单:①浓H2SO4②稀H2SO4③酸性KMnO4溶液④品红⑤Cu
任务II:实现硫元素在不同价态之间的转化。
溶液
SO2
Na2SO3溶液
Na2SO4溶液


①2Na2CO3+SO2+H2O=2NaHCO3+Na2SO3
②2NaHCO3+ SO2+H2O=2CO2↑+Na2SO3
③Na2SO3+ SO2+H2O=2NaHSO3
溶液中有关组分的质量分数变化如图是所示,图中的线2表示的组分为(填化学式)。


a.Na2S + S b.Na2SO3 + S c.Na2SO3 + Na2SO4 d.SO2 + Na2SO4