
溶液 | 盐酸 | 蔗糖水 | 草木灰水 | 石灰水 |
加入紫薯汁之后的颜色 | 红色 | 紫色 | 绿色 | 绿色 |
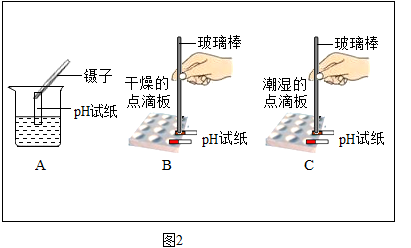
①图1中存放紫薯汁的仪器名称是。
②据上表推测,紫薯汁滴入白醋中显示的颜色是,该汁液(填“能”或“不能”)作酸碱指示剂。

仪器a的名称是。

操作B中还需用到的仪器是。
实验操作 | 现象 | 结论 |
取样品加水溶解,加入过量稀盐酸至反应完全 | 有产生 | 样品中有氯化钠 |
向上述溶液中继续滴加适量硝酸银溶液 | 有产生 |
有同学认为该实验方案有不正确,正确方案应选用(填字母)代替稀盐酸。
a.氯化钡溶液 b.稀硝酸 c.硝酸钙溶液
【方案1】取10.8g纯碱样品溶解,加入过量氯化钙溶液,搅拌至反应完全,该反应的化学方程式:。经过滤、洗涤、干燥,称量沉淀的质量为10g。计算纯碱样品中碳酸钠的质量分数为(保留到0.1%)。

a.40~10 b.60~30 c.70~40

完成下列问题:
①需要98%的浓硫酸g。
②用量筒量水时俯视读数,会导致测定炉具清洁剂中氢氧化钠的质量分数结果(选填“偏大”、“偏小”或“不变”)。