 C . 氧分子:O
D . 氧化镁中镁元素显+2价:
C . 氧分子:O
D . 氧化镁中镁元素显+2价: 提起压在容器中水面上方的活塞,容器中的水发生汽化,如图所示.下列选项中,最能表示水汽化后相同空间内粒子分布的是( ) 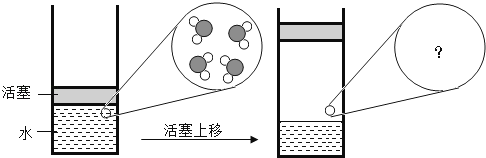
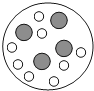 B .
B . 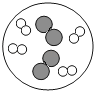 C .
C . 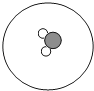 D .
D . 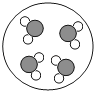
选项 | 影响因素 | 实验方案 |
A | 接触面积 | 将1g块状石灰石和20mL10%的稀盐酸、1g粉末状石灰石与20mL10%的稀硫酸混合,比较产生气泡的快慢 |
B | 催化剂的种类 | 将0.5g二氧化锰、1g氧化铁分别与10mL6%的过氧化氢溶液混合,比较产生气泡的快慢 |
C | 反应物的种类 | 分别将木炭在空气中、氧气中燃烧,比较反应的剧烈程度 |
D | 反应物的性质 | 分别用酒精灯加热表面积相同的镁片和铁片,比较在空气中能否被点燃 |
选项 | 实验目的 | 实验方案 |
A | 除去氮气中的少量氧气 | 将气体通过灼热的木炭 |
B | 验证纸张中含有碳元素 | 将纸张燃烧产生的气体通入澄清石灰水 |
C | 鉴别食盐和碳酸氢铵 | 取样,分别加热,闻其气味 |
D | 鉴别食盐水和蒸馏水 | 玻璃棒蘸取水样,分别在酒精灯火焰上灼烧,观察现象 |
![]()

a.减少石磨阻力 b.稀释豆汁浓度 c.清洗豆子
a.未用玻璃棒在漏斗内搅拌
b.滤纸未紧贴漏斗内壁
c.未先将待滤液静置,导致大量泥沙进入滤纸内堵塞小孔
新型灭菌消毒剂—ClO2
为抑制病毒传播,“含氯消毒剂”被广泛使用,其中就包含一种新型灭菌消毒剂--ClO2。在通常情况下,ClO2是一种有刺激性气味的黄绿色气体,熔点为-59℃,沸点为11℃。在常温下,1L水中大约能溶解2.9gClO2。ClO2受热或见光易分解,具有强氧化性和很强的腐蚀性。含有2%的ClO2和0.085%Na2CO3的水溶液无色、无臭、无腐蚀性,常温下稳定,不易分解;该溶液用于杀菌、消毒的同时,还有除臭、防霉、保鲜等作用,是特性优良、高效安全的消毒剂。我国从 2000 年起就逐渐用 ClO2取代氯气(Cl2)对饮用水进行消毒。

①应选择的药品是(填字母)。
a.氯酸钾和二氧化锰 b.过氧化氢溶液和二氧化锰
②应选择的发生和收集装置组合是(从上述实验装置“A~G”中选择)。
①图甲中B、C、D装置均可用作制取二氧化碳的发生装置,D装置与B、C装置相比,其突出优点是。关闭止水夹后,装置D中多孔隔板处依次观察到的现象是(如图乙所示,用字母e、f、g进行排序)。

②若选择H装置采用排空气法收集二氧化碳,验满的方法是。
③若将产生的二氧化碳通入紫色石蕊试液中,溶液变色,其原因是(写出该反应的化学方程式)。
方法一:在低温、加压条件下,将空气液化,然后将温度升高至-196~-183℃之间,使液态氮气先蒸发,剩余液态氧气储存于钢瓶里。
方法二:利用电解水的方法制取氧气,将得到的氧气干燥。在低温、加压条件下,使之转化为液态,储存于钢瓶里。
①从构成物质的微粒视角分析,在方法一空气液化过程中,主要改变的是。
②某工厂用方法二制取氧气,且所得氧气中有少量的臭氧(O3)。请推测:电解水时,正极收集的气体与负极收集的气体的体积之比(填“大于”“小于”或“等于”)1:2。

“解离”时,结构被破坏的分子是(填化学式)。
①小组同学不加催化剂,在不同温度下,用不同浓度的H2O2进行实验,记录实验现象如下表1。
50℃ | 60℃ | 70℃ | |
5% | 无明显气泡 | 无明显气泡 | 极少量气泡 |
10% | 无明显气泡 | 无明显气泡 | 少量气泡 |
15% | 无明显气泡 | 少量气泡 | 较多气泡 |
由表1可知:(填“升高”或“降低”)温度或(填“增大”或“减小”)反应物浓度可加快 H2O2的分解。
②在室温条件下,小组同学使用6.0mL30%双氧水,进行实验1.5h,记录如下表2。
资料:常见可溶性氯化物在水溶液中大都是以阳离子和氯离子形式分散的。
实验1 | 实验2 | 实验3 | |
氯化物的种类 | NaCl | MgCl2 | CuCl2 |
氯化物的质量 | 0.1g | ag | 0.1g |
放出氧气的体积/mL | 2.0 | 4.0 | 420.0 |
双氧水的分解率/% | 0.30 | 0.60 | 63.18 |
在表2中,a的值为。实验3中反应的符号表达式是。双氧水保存时应绝对避免引入的离子是(写离子符号)。

②B装置的作用是。
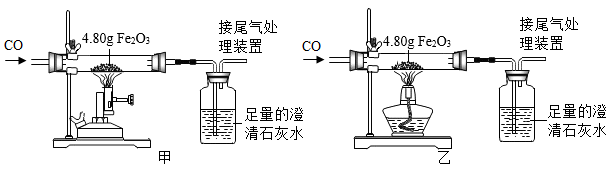
完全反应后,两组生成物均为黑色粉末(纯净物),分别用两组生成物进行如下实验:
|
步骤 |
实验操作 |
甲组 |
乙组 |
|
1 |
称量黑色粉末的质量 |
m1 |
m2 |
|
2 |
取黑色粉末,用磁铁吸引 |
能被吸引 |
能被吸引 |
|
3 |
取黑色粉末,加入稀盐酸 |
固体全部溶解,有大量气泡 |
固体全溶解,无气泡产生 |
|
4 |
取黑色粉末,加入足量硫酸铜溶液 |
有红色物质析出 |
无红色物质析出 |
①兴趣小组通过图2中甲、乙两组实验,证明对CO与Fe2O3反应的产物有影响。
②甲组所得黑色粉末与稀盐酸反应的化学方程式为。
③查阅资料发现:常温下Fe3O4不与稀盐酸或硫酸铜溶液反应。某同学猜想乙组的生成物为 Fe3O4。该同学称量黑色粉末m2=g,证实了自己的猜想。