【主要成分】雷贝拉唑钠,化学式:C18H20N3O3SNa
【用法用量】成人每日口服1次10毫克,根据病情也可每日口服1次20毫克.
【药物实验】健康成年男子分别在空腹情况下或饭后口服本药20毫克,血浆中药物浓度随时间的变化情况如图所示.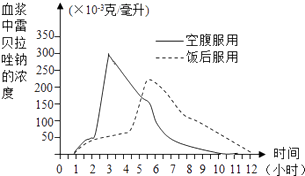
结合上述信息,回答下列问题:
实验一:鉴定是否含碳酸钙
分别取真假珍珠粉适量于两支试管中,加入一定量的稀盐酸,并将产生的气体通入中,发现都变浑浊,说明真假珍珠粉都含有碳酸钙。
实验二:鉴定是否含蛋白质
提供的器材有:相同的燃烧匙2个,酒精灯1个,火柴。小红通过实验,得出:假珍珠粉不含蛋白质。请试着写出小红的实验方案:。
资料一:过氧化钠与二氧化碳和水都能发生反应,且都放出热量。化学方程式分别为:
2Na2O2+2CO2═2Na2CO3+O2 2Na2O2+2H2O═4NaOH+O2↑
资料二:氢氧化钙的溶解度随着温度的升高而降低。
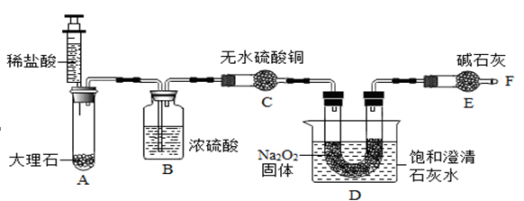
|
装置 |
A |
B |
C |
D |
E |
F |
|
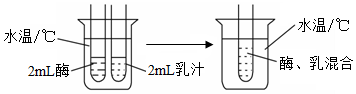
水浴温度(℃) |
10 |
20 |
30 |
40 |
50 |
60 |
|
凝乳时间( min ) |
不凝固 |
7.0 |
4.0 |
1.5 |
4.0 |
不凝固 |
|
实验操作 |
实验现象 |
实验结论 |
|
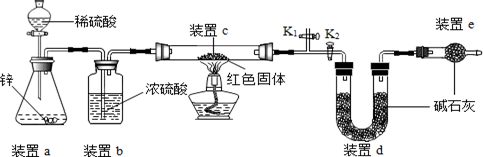
步骤1:取少量滤液于试管中,向其中滴加足量硝酸钡溶液 |
有白色沉淀生成 |
滤液中的溶质是
|
|
步骤2:静置,向上层清液中滴加无色酚酞溶液 |
溶液变红 |

|
实验次数 |
1 |
2 |
3 |
4 |
|
稀硫酸的用量/克 |
20 |
20 |
20 |
20 |
|
剩余固体的质量/克 |
20.0 |
17.4 |
14.8 |
13.5 |
分析上述数据,请回答下列问题: