A.化学与健康 | B.实验记录 |
①人体缺铁会引起贫血症 ②水果、蔬菜中富含维生素 ③用活性炭净水器可净化饮用水 | ①用10mL量筒量取7.25mL水 ②用pH 试纸测得苹果汁的pH 为3.2 ③用托盘天平称取5.6g铁粉 |
C.化学与能源 | D.安全常识 |
①煤、石油、天然气——不可再生的化石燃料 ②风能、太阳能——正在开发和利用的新能源 ③使用氢能源——可以缓解温室效应,减少酸雨 | ①厨房煤气管漏气——关闭阀门并开窗通风 ②实验时碰倒酒精灯着火——用湿抹布盖灭 ③冬天用煤炉取暖——保证室内通风 |
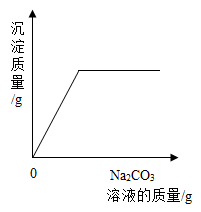 向一定量的稀盐酸和氯化钙混合溶液中不断滴入碳酸钠溶液至过量
B .
向一定量的稀盐酸和氯化钙混合溶液中不断滴入碳酸钠溶液至过量
B . 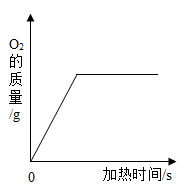 用氯酸钾和二氧化锰的混合物加热制氧气
C .
用氯酸钾和二氧化锰的混合物加热制氧气
C . 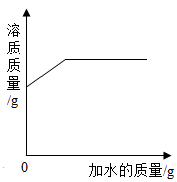 向饱和的氯化钠溶液中不断加水
D .
向饱和的氯化钠溶液中不断加水
D . 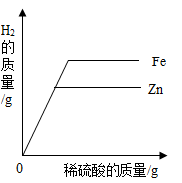 等质量的锌、铁与足量的相同溶质质量分数的稀硫酸反应
等质量的锌、铁与足量的相同溶质质量分数的稀硫酸反应
选项 | 实验目的 | 实验方案 |
A | 鉴别尿素和硫酸钾 | 取样后加熟石灰研磨,闻气味 |
B | 区别棉纤维和羊毛纤维 | 抽丝灼烧,闻气味 |
C | 除去氢氧化钠溶液中的碳酸钠 | 加适量氢氧化钙溶液充分反应后,过滤 |
D | 除去氯化钙固体中的碳酸钙 | 加足量的水溶解、过滤、洗涤、干燥 |
【查阅资料】氯化钡溶液呈中性。
实验一:取一定量白色粉末放入烧杯中,加入足量水,搅拌,静置,观察到烧杯中有白色不溶物。由此小明得出白色粉末中一定含有碳酸钙。
【讨论交流】有的同学对小明的结论提出了质疑,认为其结论不一定正确,理由是(用化学方程式表示)。
实验步骤 | 实验现象 | 实验结论 |
步骤Ⅰ:取实验一中的上层清液少量于试管中,加入过量的氯化钡溶液,过滤 | 产生白色沉淀 | 白色粉末中一定含有 |
步骤Ⅱ:取步骤Ⅰ中的滤液少量于试管中,滴加酚酞溶液 | 白色粉末中一定含有氢氧化钠 |
①步骤Ⅰ中加入过量的氯化钡溶液的目的是。
②下列物质能替代步骤Ⅱ中酚酞溶液达到实验目的的是(填序号)。
①石蕊溶液
②氧化铜
③二氧化碳
④硫酸镁溶液
⑤稀盐酸
以黄铜矿(CuFeS2)为原料,采用生物炼铜是现代炼铜的新工艺,原理为:。向上述反应后的溶液中加入Fe粉,发生两个主要反应,得到FeSO4溶液和Cu,
CuFeS2为二硫化亚铁铜,也可以表示为CuS·FeS,其中S元素的化合价为。
【探究二】探究硫酸亚铁晶体受热分解的产物
硫酸亚铁晶体(FeSO4·xH2O)是一种重要的食品和饲料添加剂,对其进行热分解研究。
查阅资料:①硫酸铜粉末为白色,吸水后变成蓝色晶体。
②二氧化硫能使高锰酸钾溶液褪色。
③硫酸亚铁晶体加热会先失去结晶水,高温会继续分解产生一种金属氧化物和两种非金属氧化物。
称取ag硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行探究,并通过称量装置B的质量测出x的值。
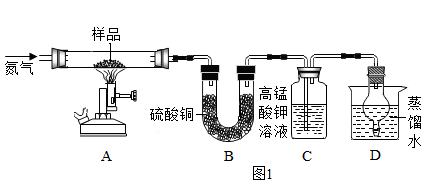
装置B中硫酸铜粉末变蓝,质量增加12.6g,说明产物中有,装置C中高锰酸钾溶液褪色,说明产物中还有;实验前后都要通入氮气。实验后要持续通入氮气,否则测出的x会(填“偏大”“偏小”或“不变”)。
