| 食物 | 鸡蛋清 | 牛奶 | 葡萄汁 | 食醋 |
| pH | 7.6~8.0 | 6.3~6.6 | 3.5~4.5 | 2.4~3.0 |
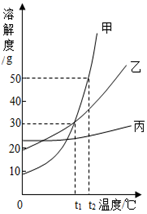
①t1℃时,甲、乙两种物质的溶解度。(填“相等”或“不相等”)
②t2℃时,甲物质饱和溶液中溶质与溶剂的质量比为。(填最简比)
③现有t1℃时甲、乙、丙三种物质的饱和溶液,将这三种溶液分别升温到t2℃,所得溶液中溶质质量分数大小关系是。(填序号)
A.甲>乙>丙 B.甲=乙<丙 C.甲=乙>丙

①反应的化学方程式为。
②小红认为小明的结论不一定正确,理由是。
③请在小明实验的基础上,选用提供的药品继续实验,判断酸和碱是否恰好完全反应,实验方案为。

①称量的氯化钠固体中含有不溶性杂质;②用量筒量取水时仰视读数;
③往烧杯中加水时有水洒出;④将配制好的溶液装入试剂瓶中时有少量溅出。