|
名称 |
84消毒液 |
洁厕灵 |
管道通 |
彩漂液 |
|
产品示例 |
| | | |
| 有效成分 | 次氯酸钠(NaClO) | 盐酸(HCl) | 氢氧化钠( NaOH ) | 过氧化氢(H2O2) |
甲烷——看不见摸不着但是很强大(节选)
据记载,我国是最早发现并使用甲烷的国家,《易经》中就谈到“象曰:泽(沼泽)中有火。”
什么是甲烷呢?
甲烷,是最简单的有机物。甲烷分子为正四面体结构(如图)。标准状态下的甲烷是一种无色无味的气体。

甲烷与全球变暖有关吗?
甲烷也是一种温室气体。甲烷的浓度对温室效应的影响如何?它与 CO2的温室效应哪个更强呢?科学家做了以下研究。
实验一:甲烷与CO2温室效应的对比探究如图,分别收集两瓶相同体积的甲烷气体和CO2气体,用温度传感器穿过塞子中间的小孔插入玻璃瓶中。将2瓶气体放在室外的阳光下,打开数据采集器,每秒采集一次数据,实验数据记录如下图:
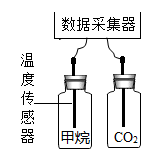
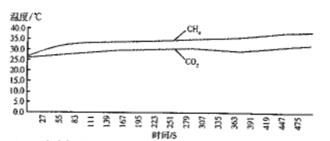
实验二:不同体积分数的甲烷的温室效应的对比探究
仍然采用实验1的方法,分别收集下列四种体积分数的甲烷样品进行实验,表中为此实验的平均值。
不同体积分数甲烷在阳光照射下的平均温度
| 甲烷体积分数 | 18% | 36% | 48% | 64% |
| 太阳光照射时甲烷的平均温度/˚C | 28.4 | 30.1 | 31.7 | 32.8 |
甲烷从哪里来?
大气中甲烷的 30%~40%是由自然源引起的,70%左右是由人类活动产生的。如:化石燃料开采过程中泄漏;种植水稻其根部的有机物质在厌氧环境下转化形成的甲烷;饲养的牛等反刍动物其食物在消化过程会产生甲烷;固体的垃圾填埋等。
回答下列问题:
(查阅资料)
a.固体酒精也被称为"酒精块"或固体燃料块。固体酒精并不是固体状态的酒精而是将酒精、硬脂酸和氢氧化钠按一定的质量比混合制成。
b.酒精的化学式为C2H5OH;
c.氯化钡、氯化钠溶液均呈中性。
d. BaCl2+Na2CO3=BaCO3↓+2NaCl 生成的BaCO3为白色固体
(提出问题)
①酒精的化学式与NaOH相比,都有“OH”,那么酒精的水溶液是不是显碱性?
②固体酒精中的氢氧化钠是否变质及变质的程度如何?
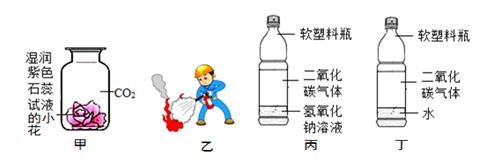
同学们取少量酒精溶液于试管中,滴加紫色石蕊溶液,未观察到紫色石蕊变为蓝色,说明酒精溶液(填“显”或“不显”)碱性。
①固体酒精中的氢氧化钠是否变质,同学们先取少量固体酒精于烧杯中,加入足量水溶解后滴加足量的稀盐酸,观察到现象,说明氢氧化钠已变质.请写出氢氧化钠在空气中变质的化学方程式。
②为进一步确定氢氧化钠的变质程度,分组进行探究。
甲组同学取烧杯上层清液于两支试管中,按如图所示进行实验。
|
实验方案 |
| |
| 实验现象 | 溶液变红 | 产生 |
| 实验结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |
乙组同学认为甲组实验不能证明清液中一定有氢氧化钠,理由是。他们另取烧杯中上层清液,加足量氯化钡溶液,充分反应后,静置,取上层清液,滴加酚酞溶液,酚酞溶液变红。
(实验结论]小组同学经过讨论,一致认为该固体酒精中的氢氧化钠部分变质。