 用一定质量的高锰酸钾加热制氧气
B .
用一定质量的高锰酸钾加热制氧气
B . 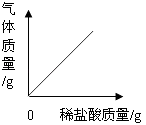 向一定质量的石灰石中加入过量的稀盐酸
C .
向一定质量的石灰石中加入过量的稀盐酸
C . 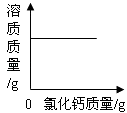 向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体
D .
向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体
D . 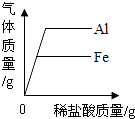 分别向等质量的铝和铁中加入溶质质量分数相同的稀盐酸至过量
分别向等质量的铝和铁中加入溶质质量分数相同的稀盐酸至过量
1799年,英国化学家汉弗菜.戴维等发现一氧化二氮能使人丧失痛觉,而且吸入后仍然可以保持意识,不会神志不清。不久后笑气就被当作麻醉剂使用,尤其在牙医师领域。因为通常牙医师无专职的麻醉师,而诊疗过程中常需要病患保持清醒,并能依命令做出口腔反应。
实验室将硝酸铵加热分解可制得一氧化二氮,硝酸铵在169.5℃熔融,在220℃分解成一氧化二氮和水。
N2O能溶于水并和水发生反应,一个笑气分子与六个水分子结合在一起。当水中溶解大量笑气时,再把水冷却,就会有晶体出现。把晶体加热,笑气会逸出,人们利用笑气这种性质,制取高纯笑气。
N2O应用于汽车工业 ,使用氮氧加速系统的改装车辆将一氧化二氮送入引擎,遇热分解成氮气和氧气,提高引擎燃烧率,增加速度。
结合短文内容和所学知识,回答下列问题:
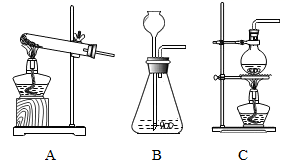
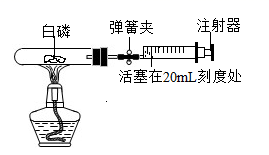
①开始实验前,该小组同学打开弹簧夹,将注射器活塞从20mL刻度处推至15mL处,然后松开活塞,观察到活塞返回至20mL刻度处。该操作的主要目的是。
②实验后,可以观察到针筒活塞会从原来的20mL刻度处慢慢向左移到约处。
a.4mL刻度
b.8mL刻度
c.12mL刻度
d.16mL刻度
③下列实验操作,对实验结果有影响的是。
a.装置漏气
b.白磷过量
c.燃烧结束后,立即松开弹簧夹,观察现象
[提出问题]为什么会生成淡黄色固体?
[查阅资料]小婧查阅资料, 记录了下列几种物质的颜色:
|
物质 |
MgO |
MgCl2 |
Mg3N2 |
Mg( NO3)2 |
Mg( OH)2 |
|
颜色 |
白色 |
白色 |
淡黄色 |
白色 |
白色 |
[初步分析]其他同学认为不可能生成上表中的,理由是。
[提出猜想]分析资料,小婧认为淡黄色固体可能是由镁与空气中的反应生成的。
[实验探究]小婧设计实验证实了自己猜想。
[实验结论]根据小婧的实验结果,写出镁条在空气中燃烧时两个反应的化学方程式:;。
[反思与评价]①空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2 , 为什么呢?请给出合理的解释。
②通过上述实验,你对燃烧有什么新的认识?。