1.
(2023高三下·曹县开学考)
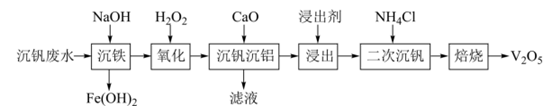
钒广泛应用于钢铁工业,钒的氧化物在化学工业常用作催化剂。某沉钒废水(含 )钒含量约为2%。从该沉钒废水中分离出铁元素并制备
)钒含量约为2%。从该沉钒废水中分离出铁元素并制备 的流程如下所示:
的流程如下所示:
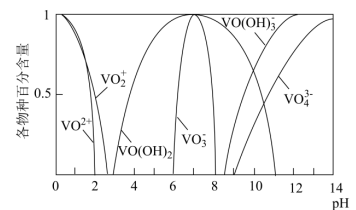
已知:①钒元素的存在形态较多,部分四价钒和五价钒物种的分布分数与pH的关系如图所示。
②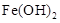 完全沉淀的pH为8.4;
完全沉淀的pH为8.4;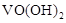 完全溶解的pH约为11。
完全溶解的pH约为11。
③吉布斯自由能( )可以用来判断反应进行的方向。一个反应的
)可以用来判断反应进行的方向。一个反应的 越小,反应发生的可能性越大。
越小,反应发生的可能性越大。
-
-
-
(2)
“沉铁”时调节pH时不能用氨水代替氢氧化钠的原因是。
-
-
-
-
(4)
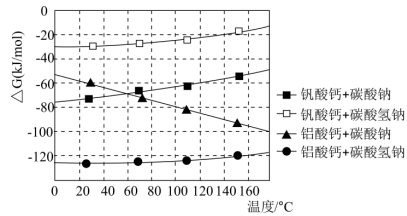
①“沉钒沉铝”中所得沉淀物与浸出剂反应

与温度的关系如图所示。“浸出”时应控制温度低于60℃,原因是
。
②若“浸出”时浸出剂中添加NaOH固体,并边浸出边通入 , 可大大提高钒的浸出率,原因是。
, 可大大提高钒的浸出率,原因是。
-
-
(5)
“二次沉钒”时,先调节pH约为6~8,得到含钒铵盐沉淀,写出“焙烧时该铵盐沉淀发生分解的化学方程式。
-


![]() 完全沉淀的pH为8.4;
完全沉淀的pH为8.4;![]() 完全溶解的pH约为11。
完全溶解的pH约为11。![]() )可以用来判断反应进行的方向。一个反应的
)可以用来判断反应进行的方向。一个反应的越小,反应发生的可能性越大。
, 可大大提高钒的浸出率,原因是。
