(3)
制备灰氢原理:
反应1:C(s)+ H2O(g)  CO(g)+H2(g) ΔH1=+131.4 kJ·mol-1
CO(g)+H2(g) ΔH1=+131.4 kJ·mol-1
反应2:CO(g)+ H2O(g)  CO2(g)+H2(g) ΔH2=-41.1 kJ·mol-1
CO2(g)+H2(g) ΔH2=-41.1 kJ·mol-1
一定温度下,在恒容密闭容器中投入足量炭粉和1 mol H2O(g)发生上述反应,起始压强为0.2 MPa。测得H2O(g)的转化率与温度的关系如图所示。
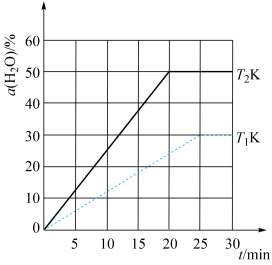
①C(s) +2H2O(g)  CO2(g)+ 2H2(g) ΔH=kJ·mol-1。
CO2(g)+ 2H2(g) ΔH=kJ·mol-1。
②T1T2(填“>”“<”或“=”)。
③T2K下,达到平衡时CO为0.1mol,此时,反应体系中(填“吸收”或“放出”)热量为kJ。
④T2K下,反应1的平衡常数Kp=MPa。(提示:用分压计算的平衡常数为Kp , 分压=总压 ×物质的量分数)
⑤T2K下,0~20min内H2的分压变化率为 MPa· min- 1。
