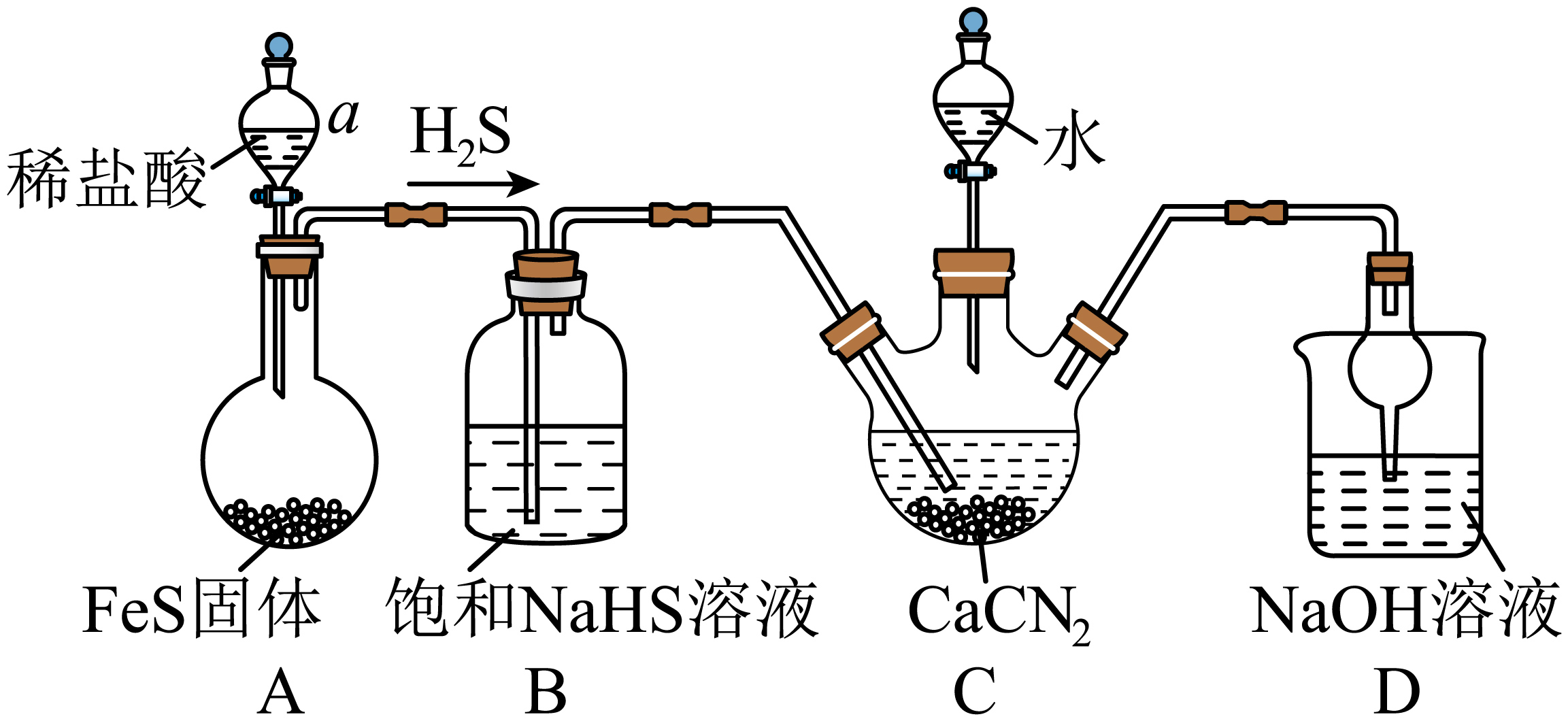
已知合成硫脲的反应原理为:
回答下列问题:
步骤1:称取20.00g产品溶于水,配制成100mL溶液备用
步骤2:向一锥形瓶中加入0.03mol碘单质和足量NaOH溶液,发生反应:
步骤3:向锥形瓶中加入10.00mL步骤1配制的溶液,发生反应:
步骤4:待步骤3反应充分后加稀硫酸,发生反应:
步骤5:以淀粉溶液作为指示剂,用1.00的
, 标准液滴定步骤4得到的溶液,发生反应:
, 平行滴定三次,消耗
标准液的平均体积为20.00mL
①判断达到滴定终点的实验现象是。
②产品中硫脲的含量为。
③下列操作会导致测得的硫脲含量偏高的是(填字母)。
A.配制溶液时,所用容量瓶未干燥
B.“步骤4”加入稀硫酸的量不足
C.盛装标准液的试管未润洗
D.滴定开始时俯视读数,达到滴定终点时仰视读数

回答下列问题:

①可看作是
中的一个O原子被S原子取代的产物,
的空间结构是。
②的晶胞是
与
构成的长方体,
在晶胞中的位置如图所示。已知晶胞的体积为V
, 阿伏加德罗常数的值为
,
晶体的摩尔体积
(列出计算式)。

I.水蒸气重整:
Ⅱ.热裂解:
Ⅲ.脱羧基:
Ⅳ.水煤气变换:
回答下列问题:

①表示水碳比(S/C)=4的曲线是(填“a”或“b”),该水碳比下制氢的最佳温度是。
②水碳比(S/C)=2时,(g)平衡产率随温度升高先增大后逐渐减小。
(g)平衡产率逐渐减小的原因可能是。
①体系中的物质的量为。
②反应Ⅱ的化学平衡常数K=。