 钻石(C)
B .
钻石(C)
B .  水晶(SiO2)
C .
水晶(SiO2)
C .  食盐(NaCl)
D .
食盐(NaCl)
D .  钟乳石(CaCO3)
钟乳石(CaCO3)
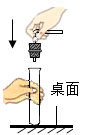 B . 检查气密性
B . 检查气密性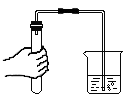 C . 加热固体
C . 加热固体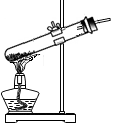 D . 氧气验满
D . 氧气验满
谈到二氧化硫,人们可能会想到它对人体健康和环境的危害。其实在食品行业,SO2是一种国内外允许使用的食品添加剂,通常以焦亚硫酸钠、亚硫酸钠等形式添加在食品中,起到护色、漂白、防腐和抗氧化的作用。
SO2常用于葡萄酒的生产加工。SO2作为保鲜剂,在低温环境下可有效减缓酿酒葡萄的腐烂。研究人员在4℃时,采用不同浓度的SO2对酿酒葡萄进行预处理,经过四周的储藏,测得酿酒葡萄的腐烂率如右图所示。葡萄酒的生产过程包括葡萄除梗、榨汁和葡萄汁发酵等步骤。葡萄汁的发酵过程是在酵母的作用下将多糖转化为酒精(C2H5OH),此过程需添加SO2抑制杂菌的滋生。
为保证SO2安全使用,我国《食品添加剂使用标准(GB2760-2014)》明确了各种食品中SO2最大残留量:
食品 | 蜜饯 | 葡萄酒 | 食糖 | 水果干 | 巧克力 | 果蔬汁 |
最大残留量 | 0.35g/kg | 0.25g/L | 0.1g/kg | 0.1g/kg | 0.1g/kg | 0.05g/kg |
世界卫生组织也规定,每人每天摄入的SO2(比体重)应控制在0.7mg/kg以内,否则人体会产生中毒现象。

依据文章内容回答下列问题。
①按照国家标准,巧克力中的SO2最大残留量为0.1g/kg。
②生产葡萄酒的步骤中,所涉及的变化均属于化学变化。

【查阅资料】
①茶多酚是一种白色粉末,略有吸水性,易溶于温水、乙醇等,在碱性环境中不稳定。
②茶汤的滋味取决于茶多酚与氨基酸的协调程度(即酚氨比),酚氨比越小,滋味越好。
【进行实验】
实验1:称取3.0g龙井茶放入瓷质盖碗中,用150mL100℃不同种类的水冲泡,5min后测定茶汤中酚氨比,实验数据如下:
水的种类 | 桶装纯净水 | 天然饮用水 | 自来水 | 井水 |
水的pH | 7.6 | 7.05 | 7.7 | 7.02 |
硬度(煮沸) | 0 | 3.08 | 3.44 | 6.43 |
酚氨比 | 6.28 | 6.82 | 6.13 | 6.32 |
实验2:用龙井茶与桶装纯净水配制茶水比为1:100的茶汤,测定不同水温及浸泡时间下的茶多酚溶解率,数据如下图所示。

茶树适宜生长在pH为4.5~6.5的土壤中,该土壤呈(填“酸性”或“碱性”)。