
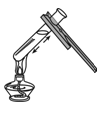
 B . 倾倒液体
B . 倾倒液体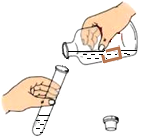 C . 检查气密性
C . 检查气密性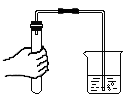 D . 稀释浓硫酸
D . 稀释浓硫酸

①净水时常用活性炭除去水中的色素和异味,说明其具有性。
②家庭中常用的方法降低水硬度。
大豆异黄酮(C15H10O4),浅黄色粉末,气味微苦,略有涩味,是大豆生长中形成的一类次生代谢产物,是一种植物雌激素,可以影响到激素分泌、代谢生物学活性、蛋白质合成、生长因子活性,是天然的癌症化学预防剂。
豆腐中含异黄酮27.74毫克,其干物质含异黄酮200毫克以上。点浆是制作豆腐的关键工序。点浆时常用到的凝固剂有盐类凝固剂,如石膏(主要成分为硫酸钙)或盐卤(如氯化镁等);酸类凝固剂,如葡萄糖酸―δ―内酯(化学式为 C6H10O6 , 简称 GdL)。
凝固剂种类对豆腐中异黄酮含量有影响。二者的关系如图1所示。
凝固剂添加量对豆腐的品质也有影响。将大豆泡发后,与水按1:4的比例磨成豆浆,以MgCl2为例,研究结果如图2所示。


豆腐中还含有丰富的蛋白质和钙,不含胆固醇,容易消化吸收。但过量食用,会阻碍人体对铁的吸收,而且容易出现腹胀、腹泻等症状。
依据文章内容回答下列问题。
①MgCl2添加的越多,豆腐的保水性越好。
②豆腐营养丰富,多吃对身体无害。
【查阅资料】维C泡腾片是一种较新的药物剂型,主要成分有:维生素C(C4H6O6)、碳酸氢钠(NaHCO3)、柠檬酸(C6H8O7)等。
维生素C主要增强机体抵抗力,用于预防和治疗坏血病。温度超过80℃被破坏。
探究1:维C泡腾片水溶液酸碱性
取1mL溶液于试管中,滴加2滴紫色石蕊溶液,发现溶液变红,说明泡腾片与水发生反应后,溶液显性。
【提出猜想】该气体可能是CO2、CO、O2、H2和N2中的一种或几种
小明认真思考后认为:从药品安全角度考虑,排除了CO和H2;从元素守恒角度考虑,产生的气体也不可能是N2 , 因为。
实验序号 | 实验操作 | 实验现象 | 实验结论 |
实验① | 操作1 | 澄清石灰水变浑浊 | 气体中含有CO2 |
实验② |
| 带火星的木条不燃烧 | 气体中不含有O2 |
补全实验报告:操作1。
【进行实验三】将泡腾片与50mL水混合,利用压强传感器测量从0s至60s时增大的压强值。
|
实验序号 |
泡腾片的数目 |
泡腾片的形状 |
温度/℃ |
60s时增大的压强值/kPa |
|
① |
4 |
每颗切成4等份 |
25 |
10.67 |
|
② |
4 |
每颗切成4等份 |
37 |
18.75 |
|
③ |
4 |
每颗研碎成粉末 |
37 |
23.58 |
|
④ |
6 |
每颗切成4等份 |
25 |
13.86 |
|
⑤ |
6 |
每颗研碎成粉末 |
25 |
20.57 |
|
⑥ |
6 |
每颗研碎成粉末 |
37 |
25.46 |
【解释与结论】
探究泡腾片形状会影响产生气体的速率的实验是(填实验序号)。
通过实验,你对维C泡腾片的保存或使用注意事项等提出一项建议。