【查阅资料】①SO2 能使品红溶液褪色;②SO2 易与高锰酸钾溶液反应而被吸收,并能使其褪色;③SO2 能使氢氧化钡溶液和澄清石灰水变浑浊;④CO 和 CO2 均不能使品红溶液褪色,也不与高锰酸钾溶液反应。
【实验研究】为验证这三种气体,同学们设计并进行如下实验:

【事实与结论】通过实验验证了以上三种气体都存在
【资料】无水硫酸铜遇到水或水蒸气变蓝色,空气中有水蒸气。

【设计实验】如下图所示,取甲、乙、丙三支洁净的试管,向甲试管中加入无水乙酸和无水硫酸铜,向乙试管中加入氢氧化钠固体和无水硫酸铜,向丙试管中加入无水乙酸、氢氧化钠固体和无水硫酸铜,并将试管内的试剂充分混合。
【实验反思】

【提出问题】废液中含有什么物质?
【假设猜想】通过分析上述实验,同学们猜想:废液中除酚酞和水外一定含有。
学生甲 | 还可能有 Ca(OH)2、NaOH | 学生丙 | 还可能有 Ca(OH)2、CaCl2 |
学生乙 | 还可能有 NaOH、Na2CO3 | 学生丁 | 还可能有 Na2CO3 |
… | … |
【查阅资料】CaCl2+Na2CO3=CaCO3↓+2NaCl
【实验验证】同学们对可能含有的物质进行确定,取一定量的废液过滤,向滤液中逐滴加入氯化钙溶液,根据反应现象绘制了如图所示的示意图。

①【结论解释】分析图象数据得出可能含有的物质中,一定含有。
②【拓展提高】那么是否含有氢氧化钠呢?请你帮他写出判断的方法:。
⑴甲小组同学的实验如下:取少量滤液放入试管中,滴加过量的氯化钡溶液,再滴加稀硝酸,观察到有白色沉淀产生,反应的化学方程式为。过滤,再向滤液中滴加,又有白色沉淀产生,最终认为乙小组观点正确。
⑵乙小组同学认为甲组同学实验方法不合理,将氯化钡溶液改成硝酸钡溶液,其余方法步骤都相同。
⑶你认为甲、乙两小组的实验设计哪个合理?并说明理由。。

A .生成 H2 的体积 a 毫升 B .反应前仪器和药品的质量 b 克
C .反应后剩余固体的质量 c 克 D .反应后仪器和药品的质量 d 克
E .黄铜样品的质量 e 克
①提出假设:该反应的气体产物全部是二氧化碳。
②设计方案:将一定量的氧化铁在隔绝氧气条件下与过量炭粉完全反应(如图),测定参加反应的碳元素与氧元素的质量比。
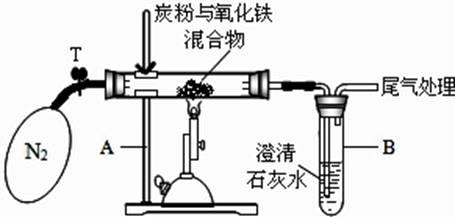
③查阅资料:氮气不与碳、氧化铁发生反应,可用来隔绝氧气。
④实验操作:
Ⅰ称取 3.2g 氧化铁与 2g 碳粉均匀混合,放入 48.48g 的玻璃管中,按如图装置连接;
Ⅱ加热前,先通一段时间纯净、干燥的氮气,其目的是;
Ⅲ夹紧 T 处弹簧夹,加热一段时间,澄清石灰水变浑浊;
Ⅳ完全反应后,冷却至室温,称得玻璃管和固体的总质量为 52.24g。
⑤数据处理:经计算,参加反应的碳元素质量为 0.48g,氧元素质量为 0.96g。
⑥得到结论:根据数据处理结果,得出原假设不成立,理由是。
石灰石样品中(已知 SiO2 不与盐酸反应),得到如下部分数据:
次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
剩余固体的质量/g | 30 | a | 20 | 15 | 15 |