
选项 | 反应 | 铝 | 镁 |
A | 与非金属 | 能被Cl2、O2氧化 | 能与N2、O2反应 |
B | 与水 | 能与沸水反应 | 反应很困难 |
C | 与碱 | 能溶于强碱溶液 | 不反应 |
D | 与某些氧化物 | 能与Fe2O3、MnO2、Cr2O3等 金属氧化物发生铝热反应 | 能在CO2中燃烧 |
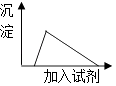
①向饱和碳酸钠溶液中通入过量的CO2; ②向 NaAlO2溶液中逐滴加入过量的稀盐酸;
③向AlCl3溶液中逐滴加入过量的稀氢氧化钠溶液; ④向硅酸钠溶液中逐滴加入过量的盐酸
①A+NaOH=D+H2O
②B=A+H2O
③C+NaOH(适量)=B+NaCl
④C+D+H2O=B+NaCl
则A是、C是(填化学式)
物 质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
颜 色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
[提出问题]为什么会生成淡黄色固体?
[查阅资料]该同学查阅资料,记录了右
表中几种物质的颜色:
(1)其他同学认为不必查阅氯化镁的颜色,理由是 ;
(2)[提出猜想]分析资料,A同学认为淡黄色固体可能是由镁与空气中的 反应生成的;
(3)[实验探究]该同学设计实验证实了自己的猜想,他的方案可能是 将点燃的镁条伸人充满氮气的集气瓶中,观察是否生成淡黄色的固体 ;
(4)[实验结论]根据该同学的实验结果,写出镁条在空气中燃烧时发生的两个反应的化学方程式: 、 ;
(5)[反思与评价]通过上述实验,你对燃烧有什么新的认识? .

②下列操作使所配溶液浓度偏大的是(填写字母)。
A.称量用了生锈的砝码
B.将NaOH放在纸张上称量
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中
D.往容量瓶转移时,有少量液体贱出
E.未洗涤溶解NaOH的烧杯
F.定容时仰视刻度线
G.容量瓶未干燥即用来配制溶液
Fe2(SO4)3净水的原理是.
使用时发现Fe2(SO4)3 并不能使酸性废水中的悬浮物沉降除去,其原因是.
在酸性环境下,向含重铬酸根的废水中加入FeSO4溶液,然后调节pH,使生成的Cr3+转化为Cr(OH)3 , 写出第一步反应的离子方程式.
①硫酸铝和氨水 ②偏铝酸钠和稀盐酸 ③硫酸锌和氢氧化钠 ④硫酸锌和氨水.