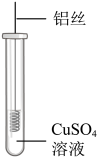
铝丝表面未出现红色物质,原因是。
填写实验报告单:
序号 | 实验现象 | 结论与解释 |
① | 铝丝表面有少量气泡;铝丝周围出现蓝绿色物质 | CuSO4溶液呈弱酸性,与Al反应产生的气体是;蓝绿色物质成分待探究 |
② | 24h后,铝丝仍光亮;48h后,铝丝表面出现少量红色物质 | 红色物质是,说明Al能和CuSO4溶液反应,但反应较慢 |
③ | 铝丝周围溶液逐渐变成无色,铝丝以下溶液仍为蓝色;两层溶液界面清晰 | 反应生成的Al2(SO4)3为无色;Al2(SO4)3溶液的密度(填“>”或“<”)CuSO4溶液的密度 |
资料:①Cu2(OH)2SO4呈蓝绿色,不溶于水;②Cl-可加快铝丝和其他物质的反应速率。
取出铝丝,将试管中的混合物分离得到蓝绿色固体。加入稀硫酸,固体溶解形成蓝色溶液,该反应的化学方程式为。
铝制品有较好的抗腐蚀性,其原因是。(用化学方程式表示)