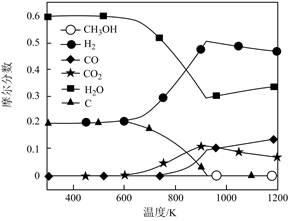
甲醇蒸汽重整制氢过程中有以下化学反应。
|
编号 |
反应 |
方程式 |
△H/kJ·mol-1 |
|
R1 |
甲醇蒸汽重整 |
CH3OH(g)+H2O(g) | △H1=+49.24 |
| R2 | 甲醇分解反应 | CH3OH(g) | △H2 |
| R3 | 水汽反应 | CO(g)+H2O(g) | △H3=-41.17 |
| R4 | 积碳反应 | CO(g)+H2(g) | △H<0 |
| CO2(g)+2H2(g) | △H<0 | ||
| 2CO(g) | △H<0 |
资料:产氢率和水碳比(S/C)的定义:
①产氢率=
②水碳比(S/C)表示反应物中H2O和CH3OH的比值,水碳比的变化是以CH3OH不变,改变H2O的物质的量加以控制。
理想产氢率=。
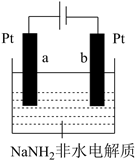
氨分子中具有较高的含氢量,因此是制氢的优选原料。使用NaNH2非水电解质研究液氨电解制氢原理,装置示意图如图所示。
资料:2NH3 NH
+NH
①某电极上发生的电极反应为6NH3+6e-=3H2↑+6NH ,该电极为(选填a或b)极。
②写出另一极上发生的电极反应。
③不考虑其它能量损耗,利用该装置产生1mol氢气时,转移电子的物质的量是mol。