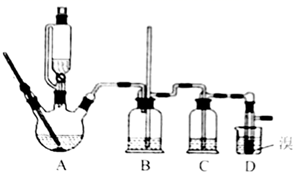
用少量的溴和足量的乙醇制备1, 2- 二溴乙烷的装置如下图所示:
有关数据列表如下:
|
乙醇 |
1, 2- 二溴乙烷 |
乙醚 |
|
|
状态 |
无色液体 |
无色液体 |
无色液体 |
|
密度/ |
0.79 |
2.2 |
0.71 |
|
沸点/℃ |
78.5 |
132 |
34.6 |
|
熔点/℃ |
-130 |
9 |
-11+ |
回答下列问题:
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
a.A的滴液漏斗的侧面导管有利于液体顺利滴落
b.B的长导管可防止反应出现堵塞情况
c.B有防倒吸作用