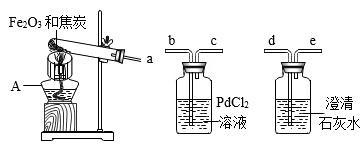
(查阅资料)①铁粉为黑色;常温下,Fe、Fe3O4可被磁铁吸引;
②PdCl2 , 溶液可用于检验CO,原理是∶PdCl2+CO+H2O=Pd↓+CO2+2HCl;
③Fe3O4与硫酸反应∶ Fe3O4+4H2SO4=FeSO4+Fe2(SO4)3+4H2O。
(实验现象)澄清石灰水变浑浊,PdCl2溶液中产生黑色沉淀,玻璃管内粉末全部变成黑色。冷却后,用磁铁靠近黑色固体,黑色固体被部分吸引。
(实验结论)反应生成CO 和CO2 , 磁铁上的黑色固体可能是 Fe、Fe3O4。
猜想一:Fe
猜想二∶ Fe3O4
猜想三∶ Fe 和Fe3O4
(设计实验)
|
设计思路 |
操作 |
现象 |
结论 |
|
定性实验 |
取少量黑色固体于试管中,加入足量稀硫酸,充分反应 |
固体完全溶解,产生气泡 |
猜想不成立 |
|
定量实验 |
取一定质量的稀硫酸(足量)放入烧杯中,加入5.6g黑色固体,充分反应后称量溶液的质量 |
固体完全溶解,产生气泡,溶液增加的质量为 |
猜想一成立 |