①20℃时,用食盐和水分别配制浓度为5.6%、15.7%、22.4%、26.5%的四种食盐水。
②将四种浓度的食盐水各取100g。放置冰箱中降温凝固,最后温度均为-25℃。
③将上述的四种冰冻食盐水移至相同环境中升温,记录各自的熔点,处理相关数据得到“冰冻盐水的熔点和浓度的关系”如图。

本实验配制溶液时,溶解过程需要用的玻璃仪器有。

【进行实验】
实验操作 | 序号 | 金属 | 实验现象 |
| ① | Zn | 60min后,滤纸上长出约1.5cm“铜树” |
② | Al | 60min后,滤纸上长出约0.8cm“铜树” | |
③ | Mg | 镁片表面有气泡产生,60min后,滤纸上得到少许细碎红色固体 |
【解释与结论】
Mg、Al和Zn三种金属能从溶液中置换出铜的原因是。

任务一 了解过碳酸钠的制备
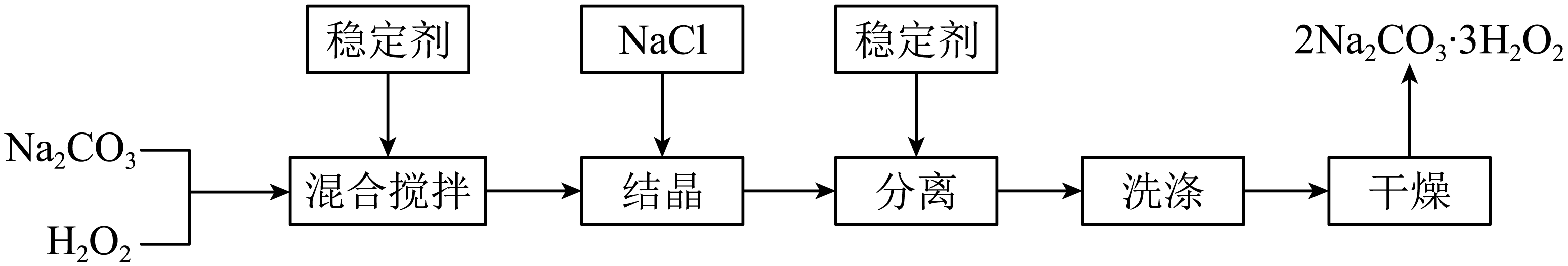
它的制备流程如上图所示,请回答下列问题:
某化学学习小组为了定性探究铁离子对过碳酸钠(2Na2CO3·3H2O2)的不良影响,取过碳酸钠固体,加入FeCl3溶液,产生大量无色无味的气体(己排除N2与H2的可能)。
【提出问题】过碳酸钠与FeCl3溶液反应后的气体是什么?
【猜想与假设】
假设1:气体只有O2;
假设2:气体只有CO2;
假设3:。
【实验探究】按如图装置对猜想进行验证:
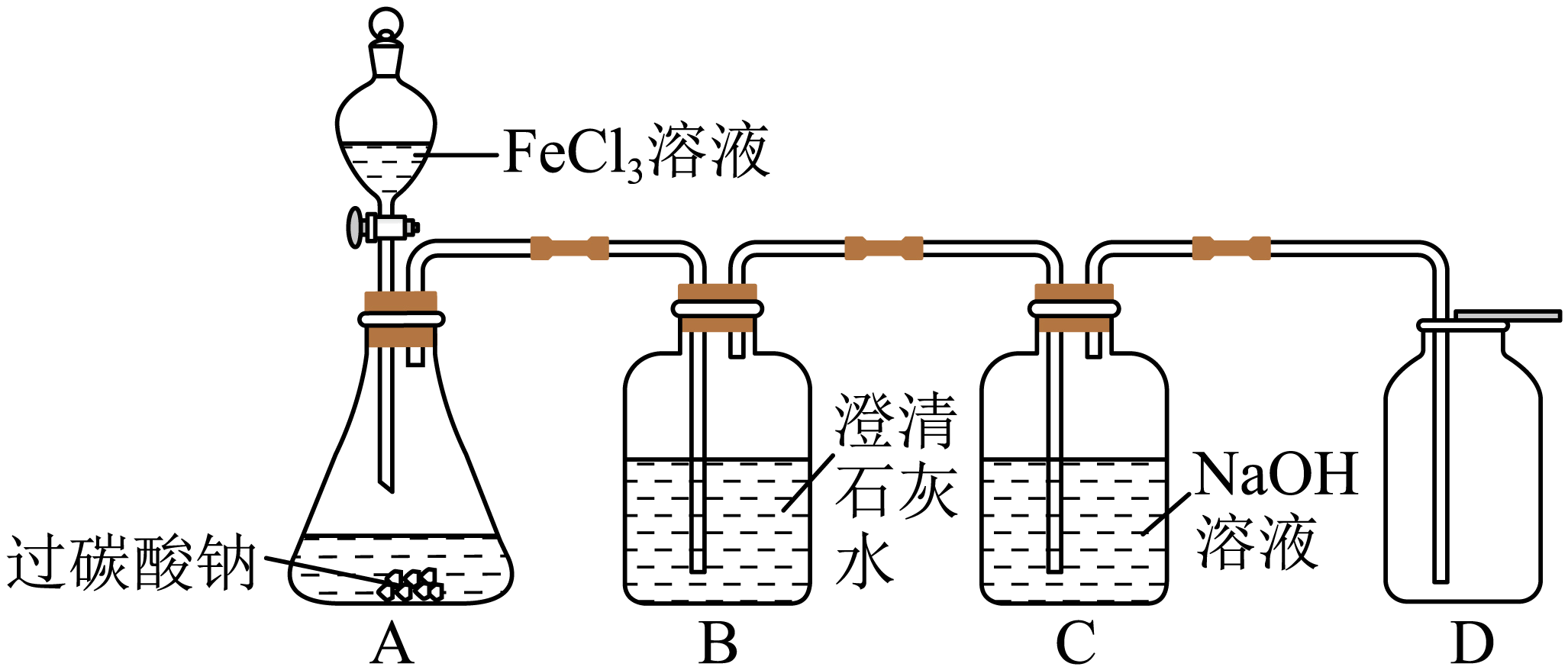
实验操作 | 实验现象 | 实验结论 |
向A中加入FeCl3溶液,将生成的大量气体依次通过B、C,再将放入D中。 | 观察到。 | 猜想3正确 |
【得出结论】过碳酸钠遇氯化铁溶液产生的气体是氧气和二氧化碳。
【交流反思】
①在上述反应中,氯化铁类似于二氧化锰,起作用,促使过氧化氢分解出氧气。
②氯化铁和Na2CO3溶液会发生反应,生成CO2 , 同时产生红褐色沉淀,写出该化学反应方程式。