一、选择题(本大题 16 个小题,每题只有一个正确答案,共 32 分)
-
1.
下列是日常生活中常发生的一些变化,其中属于物理变化的是( )
A . 水受热沸腾
B . 动物的呼吸
C . 铁锅生锈
D . 剩饭变馊
-
2.
中国火星车“祝融号”在火星表面执行的科学探测任务中,与化学有关的是( )
A . 探测火星电磁场
B . 探查火星地貌和地质构造
C . 调查火星地表气候
D . 分析火星表面的物质组成元素
-
3.
下列化学符号中,只具有微观意义的是( )
A . S
B . 2N
C . H2O
D . Fe
-
4.
下列物质中不属于化合物的是( )
A . 锰酸钾
B . 氧气
C . 冰水混合物
D . 过氧化氢
-
A . O
B . Si
C . Al
D . Fe
-
-
7.
下列变化属于化合反应的是( )
A . 红磷在氧气中燃烧
B . 铁丝放入硫酸铜溶液
C . 双氧水制氧气
D . 氧气打雷放电时转变成臭氧
-
8.
2023年是全国城市节约用水宣传周活动开展32周年。下列关于水的说法正确的是( )
A . 水资源分布不均对人类生产生活没有影响
B . 地球上的水储量极少
C . 海水中营养元素丰富建议直接饮用
D . 蒸馏水一定是软水
-
9.
下列描述的变化中,不能用质量守恒定律解释的是( )
A . 蜡烛燃烧后质量减小
B . 将3g食盐放入3g水中完全溶解后得6g溶液
C . 铁生锈后质量增加
D . 硫粉在空气中充分燃烧后固体质量减小到0g
-
10.
偶氮甲酰胺(化学式为C2H4N4O2)是一种常用的面粉改良剂,在面粉中使用可以使面包更筋道,有弹性,从而改善面包的口感,也有一定的漂白作用。下列说法正确的是( )
A . 偶氮甲酰胺中含有氧分子
B . 偶氮甲酰胺由偶氮甲酰胺分子构成
C . 偶氮甲酰胺中氧元素的质量分数最大
D . 偶氮甲酰胺中碳、氢、氮和氧四种元素的质量比为1:2:2:1
-
11.
“天为棋盘星作子,中国北斗耀太空”,最新一代原子钟——“铷原子钟”被称为北斗卫星的心脏。如图是铷元素在元素周期表中的信息,下列说法正确的是( )
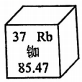
A . 一个铷原子有37个中子
B . 铷元素和铁元素的本质区别是中子数不同
C . 一个铷离子 Rb+有36个电子
D . 铷的相对原子质量是85.47g
-
12.
下图是某化学反应前后的微观示意图,下列说法错误的是( )
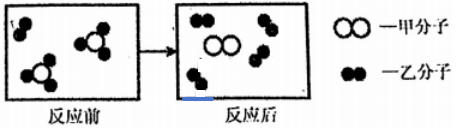
A . 生成的甲、乙分子个数比是1:4
B . 该反应为分解反应
C . 反应物的1个分子中有4个原子
D . 反应前后原子个数不变
-
13.
下列说法正确的是( )
A . 氧化物一定含有氧元素,故含有氧元素的物质一定是氧化物
B . 同种元素的粒子具有相同质子数,故Fe、Fe2+、Fe3+具有相同的质子数
C . 单质是由一种元素组成的纯净物,故由一种元素组成的物质一定是单质
D . 元素是质子数相同的一类原子的总称,故质子数相同的粒子一定属于同种元素
-
-
15.
用如图装置验证质量守恒定律。反应前称得装置及其中物质的总质量为m
1 , 引燃白磷,冷却后称得装置及其中物质的总质量为m
2。下列说法正确的是( )
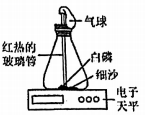
A . 该实验中白磷必须要过量
B . 实验过程中气球会一直膨胀变大
C . 若该装置气密性良好,则m1=m2
D . 反应生成 P2O5的质量等于该装置中白磷和氧气的质量之和
-
16.
下列图像能正确反映对应变化关系的是( )
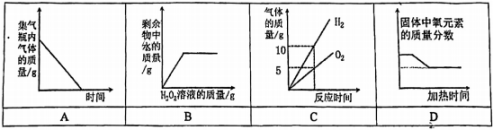
A . 碳在盛有氧气的密闭集气瓶内燃烧
B . 向一定量的二氧化锰中加入H2O2溶液
C . 电解一定质量的水
D . 用KClO3和MnO2制取氧气
二、填空题<strong><span>(</span></strong><strong><span>本大题包括</span></strong><strong><span>5</span></strong><strong><span>个小题</span></strong><strong><span>,</span></strong><strong><span>共</span></strong><strong><span>21</span></strong><strong><span> 分)</span></strong>
-
-
18.
为护航亚运会,杭州市重点整治了汽车尾气。
-
(1)
汽车尾气排放是空气污染物的重要来源,空气污染物包括有害气体(SO2 、与CO)和。
-
(2)
汽车尾气中的一氧化氮和一氧化碳在催化剂的作用下,能反应生成空气中两种无毒气体,其中一种是空气中含量最多的气体,另一种气体可参与植物的光合作用,该反应的化学方程式为 。
-
(3)
下列保护环境的措施中,合理的是____·
A . 汽车尾气处理达标后再排放
B . 农田秸秆就地焚烧
C . 生活垃圾分类处理
D . 废旧电池扔进河里
E . 亚运会主火炬首次使用废碳再生的绿色甲醇,实现循环内零碳排放
-
19.
水是一种宝贵的自然资源,某同学在学习了初中化学“自然界的水”这一学习主题后, 对相关知识整理如下:
-
(1)
净化水:自来水的生成
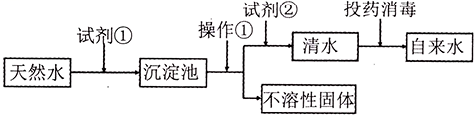
①操作①用到的玻璃仪器有烧杯、玻璃棒、。
②要检验得到的清水是硬水还是软水,可以用 (填试剂名称)。
生活中使硬水软化常用的方法是。
-
(2)
山泉水可适当的给人补充钙、钠、钾,这里的钙、钠、钾指的是____(填序号)。
A . 分子
B . 原子
C . 元素
-
(3)
探究水:电解水探究水的组成
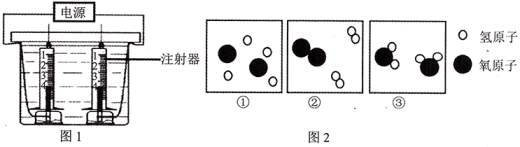
下列说法不正确的是____。
A . 反应的化学方程式为:2H2O 2H2↑+O2↑
B . 图1实验中收集气体过程中,采用俯视读数,则读数比实际体积偏小
C . 两玻璃管中收集的气体的质量比约为8:1
D . 图2为电解水的微观示意图,正确排序为③①②
2H2↑+O2↑
B . 图1实验中收集气体过程中,采用俯视读数,则读数比实际体积偏小
C . 两玻璃管中收集的气体的质量比约为8:1
D . 图2为电解水的微观示意图,正确排序为③①②
-
20.
下列是有关铜元素的化合价与对应物质类别的关系图以及相关实验装置图。
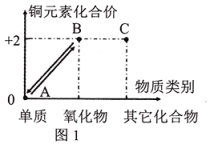
-
(1)
若物质C的化学式为CuCl2•2H2O,则其相对分子质量为。
-
(2)
过氧化氢的化学式为H2O2 , 推出过氧化铜的化学式为。
-
(3)
2023年10月26日,神舟十七号飞船发射,其中制作芯片的刻蚀液为硝酸与氢氟酸的混合溶液,工艺涉及的反应为Si+HNO3+6HF=H2SiF6+HNO2 +H2↑+X,则物质X的化学式为。
-
21.
A~F 是初中常见几种物质,它们有如图所示的转化关系,部分反应物、生成物及反应条件已省略。已知 A、B是无色液体且含有的元素种类相同,C、E是无色气体,D为淡黄色固体,F是一种由暗红色固体反应生成的白色固体。回答下列问题:
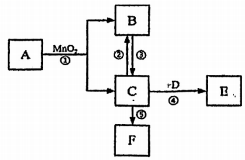
-
-
-
(3)
写出反应②的化学方程式 ,该实验中,应在水中加入少量 NaOH,其目的是。
三、实验题(本大题包括2个小题<strong><span>,</span></strong><strong><span>共</span></strong><strong><span>11</span></strong><strong><span> 分)</span></strong>
-
22.
气体制取是重要的实验活动。
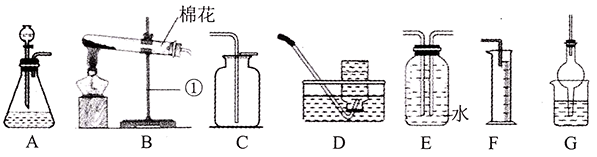
-
-
(2)
若用A装置制氧气,连接好仪器后,装入药品前需要进行的操作是,若需要收集较纯净的氧气,应选择的收集装置是(从装置A〜D中选择)。
-
(3)
若实验室用装置B制取氧气,发生反应的化学方程式为。欲收集100mL的氧气,可将装置B和E(体积为200mL)连接,若先向装置E中通入了50mL空气,则还需通入的氧气的体积为mL。
-
(4)
已知:二氧化氮具有广泛用途,是一种有毒气体,密度比空气大,易溶于水,可用氢氧化钠溶液吸收,制取原理为Cu+4HNO
3(浓)

Cu(NO
3)
2+2H
2O+2NO
2↑下列说法正确的是____。
A . 制取原理中氮元素化合价不变
B . 若将装置E没有水可用于收集NO2
C . 若用装置A制取NO2 , 仪器只需要增加酒精灯的即可
D . 收集NO2时,应将装置G中装入适量氢氧化钠溶液连接在装置末尾进行尾气处理
-
23.
兴趣小组同学进一步探究了“铁在氧气中燃烧”的实验,请回答下列问题:
提出问题:铁燃烧的产物为什么不是 Fe2O3呢?
【查阅资料】
①自然界中铁的氧化物主要是 Fe3O4(黑色)和Fe2O3(红棕色)两种,黑色FeO 极易被氧气氧化为Fe2O3。
②Fe3O4和Fe2O3的分解温度、铁的熔点见表:
| Fe3O4 | Fe2O3 | 铁 |
分解温度/℃ | 1538 | 1400 | - |
熔点/℃ | - | - | 1535 |
-
(1)
铁在氧气中燃烧时,放出大量的热,有高温物质溅落,可能炸裂集气瓶底部,因而应预先在集气瓶中,该反应的化学方程式为。
-
(2)
Fe2O3高温时会分解成Fe3O4和一种常见气体,该反应的化学方程式为。
-
(3)
根据实验现象,结合表中数据,兴趣小组分析铁在氧气中燃烧时产生高温,在该温度范围内,氧化铁已分解,所以铁在氧气里燃烧的产物不是氧化铁,你认为该温度范围应在℃之间。
-
(4)
请分析铁燃烧时溅落的高温物质中,除了Fe3O4还可能有(写化学式)
四、计算题<strong><span>(</span></strong><strong><span>本大题包括1个小题</span></strong><strong><span>,</span></strong><strong><span>共 </span></strong><strong><span>6</span></strong><strong><span>分</span></strong> <strong><span>)</span></strong>
-
24.
将13g锌粒加入足量的稀硫酸中,发生反应Zn+H2SO4=ZnSO4+H2↑,试计算:
-
-
-
(3)
生成的氢气在标准状况下的体积(标准状况下氢气的密度为0.09g/L,结果保留一位小数)。


