一、选择题(每小题只有一个选项符合题意。共<strong><span>17</span></strong><strong><span>个小题,每小题</span></strong><strong><span>3</span></strong><strong><span>分,共</span></strong><strong><span>51</span></strong><strong><span>分。)</span></strong>
-
1.
关于化学变化,下列说法错误的是( )
A . 一定产生新物质
B . 一定发生能量变化
C . 可能伴随颜色变化
D . 可能产生新的元素
-
A . 分子间隔变小了
B . 分子体积变大了
C . 分子运动加快了
D . 分子变成了原子
-
3.
某矿泉水标签上印有的主要矿物质成分及含量如下(单位为mg/L):K−3、Ca−15、Zn−0.08、Si−0.02等,这里的K、Ca、Zn、Si是指( )
A . 原子
B . 分子
C . 元素
D . 单质
-
-
5.
对实验现象的准确描述是进行科学实验探究的基础。下列有关实验现象的描述正确的是( )
A . 红磷在空气中燃烧产生大量的白色烟雾
B . 加热后木炭在空气剧烈燃烧发出白光
C . 铁丝伸入盛有氧气的集气瓶中剧烈燃烧
D . 硫在纯氧中燃烧产生蓝紫色的火焰
-
6.
下列化学用语书写错误的是( )
A . 硫酸根离子: B . 三个氢氧根离子:3OH
C . 碳酸钠的化学式:Na2CO3
D . 3个氮分子:3N2
B . 三个氢氧根离子:3OH
C . 碳酸钠的化学式:Na2CO3
D . 3个氮分子:3N2
-
7.
某同学在学习过程中发现:某原子结构示意图与其对应的化学式、化合价、离子有关联,已知镁原子结构示意图如图所示,下列说法正确的是( )
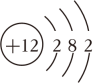
A . 镁离子符号为Mg+2
B . 氯化镁的化学式为MgCL2
C . 氯化镁中镁元素的化合价为2
D . 镁离子核外有10个电子
-
8.
下列关于化学学科基本观念的说法正确的是( )
A . 结构观——O2和O3都是氧元素组成的单质,两者的化学性质相同
B . 守恒观——化学反应前后分子、原子的种类均不变
C . 能量观——出现发热现象的一定是化学变化
D . 转化观——若燃烧后有水生成,则可燃物中一定含氢元素
-
9.
如图为电解水的实验装置图,接通电源两极都有气泡产生,实验结束发现a、b两管内气体体积比略大于2:1,下列说法正确的是( )

A . 该条件下,H2在水中的溶解度比O2的大
B . 与a玻璃管相连的电极为电源的正极
C . 打开b玻璃管活塞,点燃会产生淡蓝色火焰
D . 水通电分解的过程中,发生变化的微粒是水分子
-
10.
根据“绿色化学”的理念,某化学家设计了下列化学反应步聚:
①CaBr2+H2O CaO+2HBr
CaO+2HBr
②2HBr+Hg HgBr2+H2
HgBr2+H2
③HgBr2+CaO HgO+CaBr2
HgO+CaBr2
④2HgO 2Hg+O2
2Hg+O2
则该方案主要目的是为了制备( )
A . HgBr2
B . CaO
C . H2
D . Hg
-
11.
下列实验方案能达到实验目的的是( )
选项 | 实验目的 | 实验方案 |
甲 | 鉴别氯化钾和氯酸钾 | 取样,分别尝味道 |
乙 | 检验收集的气体是否为O2 | 用带火星的小木条伸入集气瓶中观察是否复燃 |
丙 | 鉴别CO2和N2 | 用燃着的木条,观察火焰是否熄灭 |
丁 | 检验蜡烛中是否含有氧元素 | 在蜡烛火焰上方罩一只干燥烧杯,观察现象 |
A . 甲
B . 乙
C . 丙
D . 丁
-
12.
阅读下列材料,完成下面小题。
二氧化硫在通常情况下是一种无色有刺激性气味的有毒气体,易溶于水,能使澄清石灰水变浑浊。实验室可用亚硫酸钠(Na2SO3)固体和硫酸溶液在微热条件下制备二氧化硫。
下列关于二氧化硫的说法中,不正确的是( )
A . 二氧化硫的化学式为SO2
B . 二氧化硫是由硫和氧气两种单质组成
C . 二氧化硫和亚硫酸钠中硫元素的化合价相同
D . 二氧化硫有毒,能使澄清石灰水变浑浊,属于化学性质
-
13.
下列说法正确的是( )
A . 二氧化硫和亚硫酸钠都属于氧化物
B . 实验室制备二氧化硫的反应属于分解反应
C . 实验室制取二氧化硫的装置与氯酸钾制取氧气相同
D . 实验室制备二氧化硫的化学方程式为:
-
14.
氢能源是公认的清洁能源,但氢气的制取和储存一直是一个难题。中科院煤化所与国内多家科研机构合作,采用铂﹣碳化钼双功能催化剂实现对水和甲醇的高效活化,在低温(150-190℃)下获得了极高的产氢效率。该反应过程的微观示意图如图所示,下列说法不正确的是( )

A . 该反应生成的CO2与H2的质量比为22:3
B . 铂﹣碳化钼在反应后的化学性质不发生变化
C . 该反应中各元素的化合价没有发生改变
D . 该过程使氢能源的广泛利用成为可能
-
15.
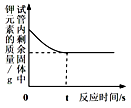
氯酸钾为白色固体,熔点为356℃,在370℃左右分解释放氧气。某兴趣小组对氯酸钾分解反应的催化剂进行研究,在相同的加热条件下,用如图装置完成表中实验:
编号 | 氯酸钾质量为/g | 催化剂 | 催化剂质量/g | 收集50mL气体所需时间/s |
实验一 | 5 | —— | —— | 171 |
实验二 | 5 | 二氧化锰 | 0.5 | 49 |
实验三 | 5 | 三氧化二铁 | 0.5 | 58 |
实验四 | 5 | 氯化钾 | 0.5 | 154 |
下列说法不正确的是( )

A . 进行实验一时,试管口应略向上倾,避免氯酸钾熔化流出
B . 用实验一再继续收集50mL氧气,所需的时间少于171s
C . 该实验收集气体时,应等到均匀冒气泡时将导管伸入量筒中
D . 实验一的作用是对照实验,三种催化剂中二氧化锰的催化效果最好
-
-
17.
硝酸铵是常用的一种氮肥,对促进植物茎、叶生长茂盛,叶色浓绿,提高植物蛋白质含量等作用。某课外活动中,小黄同学经测定某硝酸铵样品中氮元素的质量分数为28.0%,下列说法错误的是( )
A . 硝酸铵的化学式为NH4NO3
B . 该肥料样品一定是混合物
C . 硝酸铵中氮元素的化合价分别为-3价和+5价
D . 该肥料样品可能是硝酸铵和尿素【CO(NH2)2】的混合物
二、填空题(<strong><span>18-24</span></strong><strong><span>题,共</span></strong><strong><span>40</span></strong><strong><span>分)</span></strong>
-
-
19.
化学发展史上,中国科学家取得了很多伟大成就。国际标准贡献者张青莲教授主持测定了铟相对原子质量的新值,被采用为国际新标准。铟元素的原子结构示意图和在周期表中信息如图所示。

-
(1)
图2中x=,铟原子形成的铟离子是(填符号)。
-
(2)
铟位于元素周期表中第周期,相对原子质量为。
-
20.
学校运动会上短跑项目“发令枪”里的火药成分为KClO3 , MnO2和红磷,当扣动扳机时,①撞针撞击火药,产生热量使KClO3分解产生O2;②并引燃红磷产生白烟,试分别写这两步反应的化学方程式。
-
-
-
21.
小明同学对探究分子性质的实验(图1)进行了改进。如图2所示,试管丙、丁中各有一张每隔2厘米滴有一滴酚酞溶液的滤纸条,装有适量浓氨水的小药瓶固定在橡皮塞上,试管丙中小药瓶上的瓶塞已塞紧,试管丁中的小药瓶上无瓶塞。关于图1、图2中的实验有以下说法:

-
(1)
图1中(填甲、乙)烧杯变红,是因为;打开图2丙中瓶塞观察到的实验现象为,因此,图1和图2实验均能证明分子在运动。
-
-
(3)
与图1的实验相比,图2实验的优点有(任写一条)。
-
22.
水是生命之源、是自然界最重要的物质。

-
(1)
目前许多学校安装了直饮水机,其主要工作流程如图。
加热功率:32Kw 电源:220V50Hz 出水方式:1开2温1冷 过滤:二级+爱惠浦MC |
其中①中活性炭的主要作用是;③的作用是。直饮水机使用方便,只要将它与自来水管网对接,截留清除水中的有害物质(如细菌等),便得到直饮水,直饮水属于(选填“混合物”或“纯净物”)。
-
(2)
自来水厂净化水的处理过程可表示为:取水→沉降→过滤→吸附→消毒→送水。其中一定发生化学变化的是,常见净水方法净化程度由低到高为:沉淀、过滤、吸附、蒸馏,其中可将水软化,日常生活中通常用降低水的硬度。
-
23.
根据如图所示装置回答问题。

-
-
(2)
实验室用高锰酸钾制取干燥的氧气,写出该反应的化学方程式
,选择的发生装置和收集装置是
(填字母序号);若选用D装置收集氧气,收集完气体后,测得氧气的纯度明显偏低,原因可能是
(填序号)。
a.高锰酸钾中混入了氯酸钾
b.收集前,集气瓶中未注满水
c.收集后,集气瓶中仍有少量水
d.未待导管口气泡连续均匀冒出时就开始收集
-
(3)
E、F、G为木炭、硫粉和细铁丝分别在氧气中燃烧的实验操作。E中用坩埚钳夹取发红的木炭由瓶口向下(填“缓慢”或“快速”)插入集气瓶;F中潮湿的滤纸和水的作用是;G中如果没有水可能引起的后果是。
-
24.
用如图所示实验装置测定空气中氧气的含量。回答下列问题:
-
(1)
实验Ⅰ:图1是课本上的实验装置,利用红磷燃烧法测定空气中氧气的含量

图1实验中,如果红磷停止燃烧时立即记录集气瓶内水的体积,则会导致测定结果
(填“偏大”、“偏小”或“不变”)。
-
-
(3)
实验Ⅱ:图3是改进后的实验装置,利用足量的铜粉加热测定空气中氧气的含量。
图3中小气球的作用是。
-
(4)
图3实验中,为了使氧气反应更充分,实验中采取的措施合理的是____(填序号)。
A . 铜粉平铺在玻璃管中
B . 反复推拉注射器的活塞
C . 增加铜粉的质量
-
(5)
图3装置中硬质玻璃管的体积为30mL,反应前注射器活塞位于20mL刻度处,反应完毕后,最终注射器活塞停留于11mL刻度处,则该实验测得空气中氧气的体积分数为。小明分析该实验结果与理论值有差异的可能原因是。(答一条)
三、计算题(<strong><span>25-26</span></strong><strong><span>题,共</span></strong><strong><span>9</span></strong><strong><span>分)</span></strong>
-
25.
高铁列车车厢是密闭的空间,因此需要提供清洁的空气和保持车厢的卫生。高铁酸钠(Na2FeOx)是高铁上常用的一种“绿色、环保、高效”的消毒剂。
-
(1)
已知高铁酸钠的相对分子质量为166,则x的值为。
-
-
-
26.
化学兴趣小组的同学为测定实验室里一瓶体积为600mL过氧化氢溶液中H
2O
2的质量,用量筒量取60mL进行了相关实验,实验数据记录如下:过氧化氢溶液68g+二氧化锰3g

固液残留物69.4g,请计算:
-
-
(2)
计算原过氧化氢溶液中H2O2的质量(写出计算过程)。


 B .
B . 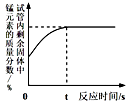 C .
C .  D .
D .