一、选择题(本题包括14小题,每小题3分,共42分)
-
1.
下列物质的用途中,利用了物质的物理性质的是( )
A . 氧气供给呼吸
B . “干冰”用于人工降雨
C . 铁粉用作包装食品“除氧剂”
D . 熟石灰用于改良酸性土壤
-
2.
如图是元素周期表的一部分,以下表述正确的是( )
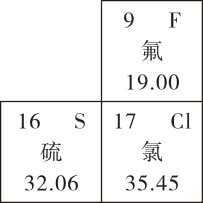
A . 氟原子的结构示意图为: B . 硫原子的相对原子质量为 32.06g
C . 氟元素和氯元素处于同一周期
D . 硫元素和氯元素具有相似的化学性质
B . 硫原子的相对原子质量为 32.06g
C . 氟元素和氯元素处于同一周期
D . 硫元素和氯元素具有相似的化学性质
-
3.
下列关于水的说法不正确的是( )
A . 自来水厂净水过程中明矾做絮凝剂,能吸附水中悬浮的杂质
B . 鉴别硬水和软水可用肥皂水
C . 蒸馏过程需放入碎瓷片防暴沸
D . 电解水过程正、负极产生气体的质量比为 2:1
-
4.
新型冠状病毒的预防和治愈都离不开化学知识,下列材料不属于有机高分子材料的是( )
A . 无纺布医用口罩
B . 水银玻璃温度计
C . 装消毒液用的塑料瓶
D . 橡胶手套
-
5.
“宏观﹣微观﹣符号”三重表征是化学独特的表示物质及其变化的方法。某化学反应的微观示意图如图所示,下列说法不正确的是( )
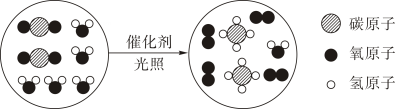
A . 从微观构成看:四种物质均由分子构成
B . 从物质分类看:该反应过程涉及到 2 种氧化物
C . 从反应类型看:该反应属于置换反应
D . 从微粒个数关系看:该反应两种反应物的分子个数比为 2:1
-
6.
下列说法错误的是( )
A . 二氧化碳灭火器在使用时手要握在木柄上,防止冻伤
B . 不慎将氢氧化钠沾到皮肤上,应先用大量水冲洗,然后涂上 3%的硼酸溶液
C . 滴加洗涤剂能将餐具上的油污洗掉,因为洗涤剂能溶解油污
D . 铁是人体所必须的微量元素,缺铁会导致贫血
-
7.
青蒿素(Artemisinin)是治疗疟疾耐药性效果最好的药物,它的分子式为 C15H22O5 , 下列关于青蒿素的说法正确的是( )
A . 青蒿素属于有机高分子化合物
B . 青蒿素中碳元素的质量分数为 20.5%
C . 青蒿素中C、H、O 元素的原子个数比为 15:22:5
D . 青蒿素中含有氢气分子
-
8.
下列关于能源的说法,不正确的是( )
A . 煤、石油、天然气和酒精都是不可再生资源
B . 化石燃料燃烧会造成空气污染
C . 氢能,风能,太阳能属于清洁能源
D . 炒菜时,天然气的火焰呈黄色,锅底出现黑色物质,是因为天然气未充分燃烧
-
9.
将一枚洁净的铁钉放入稀盐酸中,下列叙述不正确的是:( )
A . 铁钉表面有气泡产生
B . 液体由无色逐渐变为黄色
C . 溶液的质量增加
D . 该反应符合质量守恒定律
-
10.
(NH4)2SO4 是一种常见的化肥,其水溶液呈酸性,下列关于(NH4)2SO4 的说法,正确的是( )
A . (NH4)2SO4 是一种复合肥
B . (NH4)2SO4 溶液能使紫色石蕊溶液变蓝
C . (NH4)2SO4 属于酸,长期使用会导致土壤酸化
D . (NH4)2SO4 和 K2SO4 可用加熟石灰混合研磨后扇闻气味法进行鉴别
-
11.
t
2℃时,向盛有 10g 水的烧杯中加入 13g 固体甲,搅拌后固体完全溶解,放置一段时间后,溶液中固体析出,甲的溶解度曲线如图所示。若不考虑水分蒸发,下列说法正确的是( )
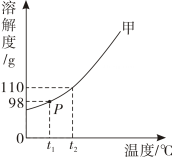
A . 甲溶于水的过程放热
B . 搅拌可以増大甲物质的溶解度
C . 甲的溶解度为 98g
D . 通过升温可以将甲的不饱和溶液变为饱和溶液
-
12.
为了达到实验目的,下列实验方案合理的是( )
|
选项
|
实验目的
|
实验试剂或操作
|
|
A
|
除去碳粉中混有铁粉
|
加入适量硫酸铜溶液,充分反应后过滤
|
|
B
|
除去氯化钠中混有的碳酸钠
|
加入过量稀硫酸,充分反应后蒸发结晶
|
|
C
|
除去氢气中混有的一氧化碳
|
通入适量氧气,再将气体点燃
|
|
D
|
除去硝酸铜溶液中混有的硝酸银
|
加入足量铜粉,充分反应后过滤
|
A . A
B . B
C . C
D . D
-
13.
向盐酸和氯化钙的混合液中逐滴滴入碳酸钠溶液,溶液 pH 随加入碳酸钠溶液质量的变化如图所示,其中氯化钙的水溶液呈中性,以下说法正确的是( )
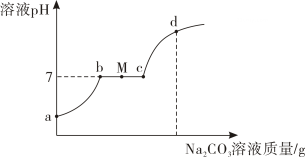
A . ab 段代表碳酸钠与氯化钙发生反应
B . M 点表示的溶液中阳离子有 Na+和 Ca2+
C . ac 段表示的溶液中溶质 NaCl 的质量先增加后减少
D . d 点处的溶液遇无色酚酞不变色
-
14.
下列实验操作对应的现象和结论不正确的是( )
|
|
实验操作
|
现象
|
结论
|
|
A
|
向某待测液中加氯化钙溶液
|
有白色沉淀生成
|
该溶液为AgNO3溶液
|
|
B
|
将CO通入灼热的氧化铁粉末中
|
粉末由红色变为黑色
|
CO有还原性
|
|
C
|
将2根铜丝分别放入硫酸铝溶液和硝酸银溶液中,观察现象
|
硫酸铝溶液没有明显现象,硝酸银溶液逐渐变蓝,其中铜丝表面有银色物质析出
|
金属活动性顺序:Al>Cu>Ag
|
|
D
|
将铜片和黄铜片相互刻画
|
铜片上留下划痕,黄铜片无明显现象
|
合金硬度比组成它的纯金属硬度大
|
A . A
B . B
C . C
D . D
二、填空题(本题包括 3 小题,共 21 分)
-
15.
类价二维图反映的是元素的化合价与物质类别之间的关系,构建类价二维图是化学学习的重要方法。图 1 是某同学绘制的关于硫元素的类价二维图。

-
-
(2)
类价二维图中的物质在一定条件下可以相互转化,煤炭中的硫元素一定条件下会转化为硫化氢和二氧化硫,两种气体混合发生反应,微观示意图如图 2 所示,请画出丁中的微粒示意图。该反应过程(填“有”或“没有”)元素的化合价发生变化。
-
(3)
二氧化硫在空气中可以通过下列转化形成硫酸型酸雨:
① ; ②。
; ②。
-
16.
有一包固体样品,可能含碳酸钠、硫酸铁、氢氧化钠、氯化钡中的一种或几种。某兴趣小组为探究其成分做了以下实验:
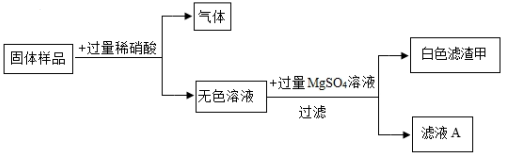
已知:氯化钡的水溶液呈中性。
-
(1)
向固体样品中加入过量稀硝酸,产生的气体是(写化学式),产生白色滤渣甲的化学方程式为:;
-
(2)
原样品中一定有,一定没有,可能含有;(写化学式)
-
(3)
滤液 A 中一定含有的阳离子是;(写离子符号)
-
(4)
若要进一步确定样品的组成,还需进行的实验操作是:(简述操作过程,现象和结论)。
-
17.
溴酸镉[Cd(BrO
3)
2]常用做分析试剂、生产荧光粉等。以镉铁矿(主要成分为 CdO
2、Fe
2O
3以及少量的 Al
2O
3和 SiO
2 , 其中 CdO
2 的含量为 72 %)为原料制备[Cd(BrO
3)
2]的工艺流程如下,已知流程中加入 CH
3OH 还原镉是将镉元素的化合价降低。回答下列问题:

-
(1)
为提高镉的浸取率,酸浸时可采取升温,增大酸的浓度或的方法来提高反应速率;
-
(2)
酸浸时 CdO2发生反应的化学方程式为:;
-
(3)
调 pH 时可向溶液中加入适量含(填离子符号)的溶液,滤渣 1 的主要成分为 Fe(OH)3、 (填化学式);
-
(4)
滤液 1 中可回收利用的主要物质是 (填化学式);
-
(5)
2000 kg 镉铁矿经上述制备流程,可制得含溴酸镉 95%的产品质量最多为 kg。(结果保留小数点后 1 位)
三、实验题(本题包括 3 小题,共 27 分)
-
18.
下图为初中化学实验室常见的仪器装置,请回答下列问题。

-
-
(2)
实验室可用 B 装置来制取 O2 , 写出反应的化学方程式:。
-
(3)
实验室常用装置 C 代替装置 B 制取气体,装置 C 的优点是可以控制反应的开始和停止,利用装置 C 控制反应停止的方法是:
(填写正确的字母顺序),反应就停止了。
a、液面低于隔板,与固体脱离接触 b、关闭弹簧夹 M c、U 型管右边液面下降
下列反应不适用于装置 C 的是(填字母)。
A、块状大理石和稀盐酸反应制取二氧化碳气体
B、锌片和稀硫酸反应制取氢气
C、高锰酸钾粉末和浓盐酸反应制取氯气(Cl2)
-
(4)
实验室用加热无水醋酸钠和碱石灰的固体混合物来制取甲烷气体,则应选择的发生装置为(填字母编号);若用装置 D 收集甲烷气体,气流方向为 进出(填“a”或“b”)。
-
(5)
以下说法正确的是____
A . 装置 A 和装置 B 的气密性检查的操作方法相同
B . 装置 B 发生反应时,仪器②下端需浸没在液体中
C . E 装置可用于干燥气体,气流方向为 c 进 d 出
D . 若挤压 F 中试管上方的滴管,可以观察到 U 型管左边液面上升
-
19.
已知:①NH
4HCO
3在 40℃受热易分解;
② ,
,
③20℃时,NaHCO3、NH4HCO3的溶解度见下表。
|
物质
|
NaHCO3
|
NH4HCO3
|
|
溶解度/g
|
9.6
|
21
|
-
(1)
在 20℃时,称取 15g NH
4HCO
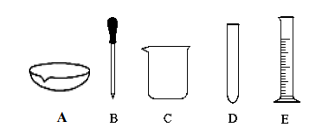
3加入 50mL 水(水的密度为 1g/mL)中,充分溶解,得到
溶液(填“饱和”或“不饱和”),此时溶液的质量分数为
(只列计算式),实验过程中不需要的仪器是
(选填字母编号)。
-
(2)
将(1)中配制的溶液平均分为 2 等份,向第一份溶液中加入足量 NaCl 固体,则最终析出 NaHCO3的质量为g(结果保留小数点后 1 位),向第二份溶液中加入适量稀盐酸,发现产生大量气泡,写出反应的化学方程式:;
-
(3)
为探究(2)中 NaHCO
3析出的最佳条件,完成了以下几组实验(其中 T
1<T
2<T
3):
|
实验序号
|
反应温度/℃
|
反应时间/min
|
NaHCO3产率/%
|
|
a
|
T1
|
60
|
86.8
|
|
b
|
T1
|
120
|
92.1
|
|
c
|
T2
|
60
|
X
|
|
d
|
T2
|
120
|
92.5
|
|
e
|
T3
|
60
|
85.3
|
|
f
|
T3
|
120
|
85.6
|
①实验 a 和 b 的结论是;
②表格中 X 的数值可能是(选填字母编号);
A.85.8
B.86.8
C.89.4
D.92.6
③在相同反应时间,T3℃时碳酸氢钠的产率比 T1℃和 T2℃时都低,据此推测 T3≥。
-
20.
研究物质的分类对其性质和变化的规律有重要指导作用。
-
(1)
硫酸铜和硫酸钠的水溶液都可以和含(填离子符号)的盐溶液反应,产生的相同现象是;
-
(2)
已知亚硒酸钡(BaSeO
3)是一种难溶于水的白色固体,可溶于稀盐酸,亚硒酸钡可用做玻璃工业的脱色剂及制红玻璃等。
①亚硒酸钡(BaSeO3)与稀硝酸反应可生成硒酸钡(BaSeO4),硒酸钡(BaSeO4)中硒元素的化合价为:,写出硒酸的化学式:;
②依据各物质之间的反应规律,设计两种制备亚硒酸钡(BaSeO3)的方案(要求依据两种不同的反应规律)。完成下表:
|
方案
|
操作
|
预期反应的化学方程式
|
|
①
|
往盛有 Na2SeO3溶液的烧杯中滴加足量溶液,充分反应后,(填操作名称)。
|
|
|
②
|
往盛有的烧杯中滴加足量溶液,充分反应后,后续操作同上。
|
|


,
