①取一定量的白色粉末加入足量水,得到无色溶液。
②向①所得溶液中加入过量Ba(OH)2溶液,产生白色沉淀,过滤,往沉淀中加入足量稀硝酸,沉淀部分溶解。
③往②滤液中先加入几滴无色酚酞溶液,溶液变红,然后加入过量稀盐酸,再滴入几滴硝酸银溶液,产生白色沉淀。
下列关于该白色粉末成分的判断,正确的是( )
①“其底铺薪”指用燃烧的薪将煤炭引燃,从燃烧条件分析,“燃烧薪”的作用是。
②文中“倭铅”的主要成分是(填字母序号)。
A.铅B.锌C. 铅锌合金
目前汽车使用的燃料主要是汽油,它燃烧后不仅会产生二氧化碳,还会释放多种有害物质。开发能够取代汽油的新能源,研发、生产和使用环保、污染的绿色汽车都是实现“碳中和”的有效措施。研发绿色环保汽车,主要有以下途径:一是改进现有车型,采用铝合金、钛合金、塑料等轻量化材料;二是开发汽车代用燃料,主要包括天然气、乙醇、生物柴油、氢气等,实现能源多元化:三是大力发展电动汽车,尤其是鱼燃料电池汽车。
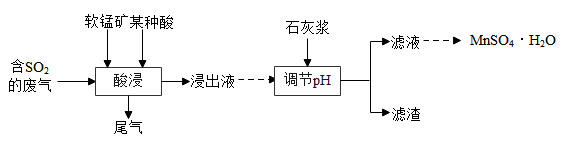
Ⅰ.不溶于水,不与酸反应。
Ⅱ. 酸浸过程中MnO2发生的主要反应为:
Ⅲ. 部分金属阳离子生成氢氧化物沉淀的pH范围如下(开始沉淀~完全沉淀);
Fe3+:1.8~3.2 Al3+:4.1~5.0 Mn2+:8.3~9.8 Mg2+:9.4~12.4
生产中将软锰矿粉碎的目的是。

a. 乙醇b. 水(常温)c.饱和MnSO4溶液
序号 | 实验内容 | 现象或结果 |
Ⅰ | 将硫酸铜溶液滴入氢氧化钠溶液中 | 产生色沉淀 |
Ⅱ | 将硫酸铜溶液滴入(填“氯化钡或“氯化钾”)溶液中 | 产生白色沉淀 |
Ⅲ | 取打磨后的铝丝放入硫酸铜溶液中 | 铝丝表面有少量气泡产生,析出红色固体,溶液逐渐变成无色 |
Ⅳ | 用测量硫酸铜溶液的pH值 | pH=5 |
小组同学讨论后认为:硫酸铜溶液的pH=7,溶液呈酸性,可推知溶液中含有(填离子符号),因此实验Ⅲ中产生的气体可能是氢气。

U形管液面出现左低右高现象的原因可能是。
加热至1000℃时CuO开始分解,该反应的化学方程式为。