|
选项试剂 |
A |
B |
C |
D |
|
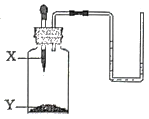
X |
H2O |
H2O |
H2O |
盐酸 |
|
Y |
NaOH |
NH4NO3 |
生石灰 |
Na2CO3 |
①生石灰 ②浓硫酸 ③氢氧化钠 ④食盐水 ⑤浓盐酸 ⑥石灰水
选项 | X的物质类别 | 稀硫酸的性质描述 |
A | 金属 | 若X为Cu,则Y一定为H2 |
B | 金属氧化物 | 若X为Fe2O3 , 则盐一定为FeSO4 |
C | 碱 | Y一定为H2O |
D | 盐 | 生成的盐一定为白色沉淀 |

①所配稀盐酸中溶质的质量为g,所需浓盐酸的质量为g。
②已知浓盐酸密度为1.19g/cm3 , 量取上述所需浓盐酸用到的仪器是(填标号)。
A、10mL量筒
B、50mL量筒
C、试管
D、胶头滴管
③测定所配稀盐酸的酸碱度,应将pH试纸放置在上。
①铁与稀盐酸反应的化学方程式为。
②下列示意图中,与实验结果相符的是(填标号)。

A熟石灰 B氯化钠 C氢氧化钠 D稀盐酸 E碳酸钠
①改良酸性土壤,配制波尔多液的是;
②侯氏制碱法中的“碱”是;
③可用来除去热水瓶中水垢的是;

①能产生气泡的是(填序号)。
②能证明C中发生反应的现象是。
③E烧杯中的物质与稀盐酸反应的化学方程式。
①浓硫酸、浓盐酸应当密封保存,原因是。
②铁桶能存放氢氧化钠溶液,不能存放稀盐酸。原因是(用方程式表示)。
①盐酸常用于除去铁制品表面的锈,反应的化学方程式是。使用盐酸时要小心,不小心溅到了手上,应当立即,再涂上3%-5%的碳酸氢钠溶液。
②下列物质中可用作治疗胃酸过多的胃药有(填序号)。
A.Al(OH)3 B.CaCO3粉末 C.NaCl D.NaOH E.CuO
写出上述胃药中碱与胃酸反应的化学方程式,选择一种不能治疗胃酸过多的物质,说明不能使用的理由。
营养液A | 营养液B | |||
肥料名称 | 硝酸钙 | 硝酸钾 | 磷酸二氢铵 | 硫酸镁 |
溶质的质量分数(%) | 9.45 | 8.08 | 1.53 | 4.93 |
【收集证据】
1组同学测定营养液A的pH,操作是,测得其pH7(填“>”“<”或“=”),证明营养液A呈中性。
【质疑评价】鹏鹏对2组同学的结论产生了质疑,理由是。为证明2组同学的结论正确,应将操作方法修改为。
【分析交流】浓缩营养液不能直接用于蔬菜种植,需加水稀释:取营养液Al0g,向其中加入990g水,稀释后溶液中溶质的质量分数是%,稀释过程中用到的玻璃仪器有:烧杯、量筒、。
同学们进行完上述活动后,将剩余的营养液A敞口放在窗外,儿天后打扫卫生时发现,营养液A中出现了少量晶体,这是为什么呢?
【查阅资料】硝酸钙在不同温度下的溶解度如下表所示:
|
温度℃ |
0 |
10 |
20 |
30 |
40 |
50 |
|
溶解度/g |
102 |
115 |
129 |
138 |
149 |
189 |
【小组讨论】原营养液A属于硝酸钙的溶液(填“饱和”或“不饱和”)。将其敞口放在窗外,出现晶体的原因可能是。


【猜想与假设】猜想一:酚酞、NaCl;猜想二:酚酞、NaCl、(填化学式);
【反思与评价】小明认为还可以用其它物质来检验无色溶液中溶质的成分。该物质可以是下列物质中的____(字母填序号)。