
根据上述实验现象能得出关于金箔中金原子结构的一些结论,试写出其中的一点:;
请回答下列问题:
[查阅资料]成人每天食用食盐的质量通常为6 g,
某种加碘食盐的标签如图所示。

[问题分析]500 g该品牌食盐中,含碘的最大质量是;若要使人体甲状腺中的碘达到饱和,至少需要一次性食用该品牌碘盐。
[结论]日常服用加碘食盐(填“能”或“不能”)起到避免核辐射的目的,原因是。
【情景提供】19世纪以前,人们一直以为原子是不可分的,直到1887年,汤姆生发现了带负电的电子后,才引起人们对原子结构模型的探索。
【提出问题】电子带负电,原子不带电,说明原子内存在带正电荷的部分,它们是均匀分布还是集中分布的呢?
【进行实验】1910年英国科学家卢瑟福进行了著名的粒子轰击金箔实验。实验做法如图所示:
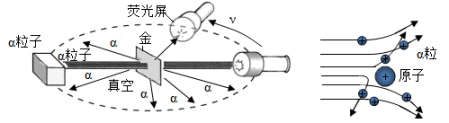
①放射源——放射性物质放出粒子(带正电荷),质量是电子质量的7000倍;
②金箔——作为靶子,厚度1μm,重叠了3000层左右的原子;
③荧光屏——粒子打在上面发出闪光;
④显微镜——通过显微镜观察闪光,且通过360度转动可观察不同角度粒子的到达情况。
【收集证据】绝大多数粒子穿过金箔后仍沿原来的方向前进,但是有少数
粒子却发生了较大的偏转,并且有极少数
粒子的偏转超过90°,有的甚至几乎达到180°,像是被弹了回来。
【猜想与假设】粒子遇到电子后,就像飞行的子弹碰到灰尘一样运动方向不会发生之明显的改变,而结果却出乎意料,除非原子的大部分质量集中到了一个很小的结构上,否则大角度的散射是不可能的。
【解释与结论】
若原子质量、正电荷在原子内均匀分布,则极少数粒子就(填“会”或“不会”)发生大角度散射。卢瑟福所说的“除非原子的大部分质量集中到了一个很小的结构上”中的“很小的结构”指的是。
请分析上述信息,回答下列问题:
①相对分子质量;
②氧元素的质量分数为(计算结果精确到0.1%)。
①少喝各种饮料,日常饮水以白开水为主
②经常吃方便面、面包等速食食品以适应我们快节奏的生活
③尽量少用塑料制品直接接触热的、含油脂的食物
④呼吁政府完善食品安全监督检验机制,严惩不法黑心业者
|
名称 |
甲烷 |
乙烷 |
丙烷 |
丁烷 |
戊烷 |
十一烷 |
十六烷 |
|
化学式 |
CH4 |
C2H6 |
C3H8 |
? |
C5H12 |
C11H24 |
C16H34 |
|
沸点/℃ |
-164 |
-88.6 |
-42.1 |
-0.5 |
36.1 |
194.5 |
287.5 |
|
相对密度 |
0.466 |
0.572 |
0.585 |
0.579 |
0.626 |
0.741 |
0.774 |
分析上表中的信息,回答下列问题。