温度/℃ | 10 | 20 | 30 | 40 | 50 | |
溶解度/g | 甲 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
乙 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | |
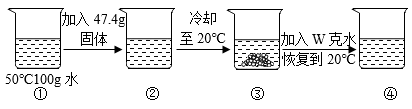
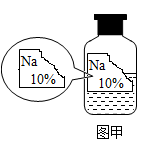
【资料查阅】上述 4 种物质的相关信息如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下稀溶液的 pH | 7 | 13 | 11 | 9 |
【实验探究 1】如图乙所示:
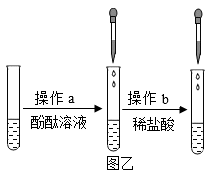
分析 4 种物质的相关信息,你认为该溶液中的溶质可能是上述 4 种物质中的,你的判断依据是;
【实验探究 2】
实验步骤 | 实验现象 | 实验结论 |
向操作a后试管中的溶液中滴加过量 CaCl2溶液(中性) | 试管中 | 溶质是 NaOH |
①如图乙所示,在操作b 滴加稀盐酸后,发现溶液由红色变为无色,为确定此时所得无色溶液中溶质的成分,可选用下列药品中的(填序号);
A.碳酸钠溶液 B.氢氧化钠溶液 C.硝酸银溶液 D.铁
②造成操作 b 中有无色无味气体产生,是因为原破损标签溶液与空气中的物质发生了如下化学反应(用化学方程式表示)。