 风力发电
B .
风力发电
B .  海水晒盐
C .
海水晒盐
C .  菜刀生锈
D .
菜刀生锈
D .  榨取果汁
榨取果汁
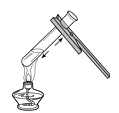 加热液体
B .
加热液体
B .  稀释浓硫酸
C .
稀释浓硫酸
C . 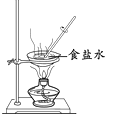 蒸发食盐水
D .
蒸发食盐水
D .  检查装置气密性
检查装置气密性

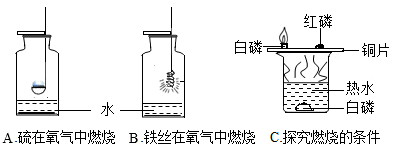
请回答:
①实验A中水的作用是。
②实验B中水的作用是。写出该反应的化学方程式。
③实验C中的水除了提供热量之外,还起到了作用。

其中活性炭起作用:紫外线起杀毒灭菌作用:超滤膜可以让水分子通过,其他大分子污染物则被截留,这个分离过程属于(填“物理”或“化学”)变化。
①抑制水中所有动、植物的生长:②不任意排放工业废水:③大量使用化肥农药:④生活污水经过净化处理后再排放。

②过氧化氢常温下不稳定,实验室用过氧化氢制取氧气的化学方程式为。
③过氧化钙,白色固体,难溶于水。与水反应缓慢释放氧气,同时生成一种碱,反应的化学方程式为。
实验步骤 | 实验操作 | 实验现象 | 结论 |
步骤1 | 取2g白色固体放入试管中,加入20mL水,充分振荡。 | 液体浑浊, 有持续的细小气泡冒出。 | |
步骤2 | 静置,取步骤1的试管上层清液少许,滴加无色酚酞。 | 无色酚酞变红。 | |
步骤3 | 该消毒剂的成分不是过碳酸钠。 |
【猜想】草酸亚铁晶体分解会产生CO、CO2和H2O三种气体。
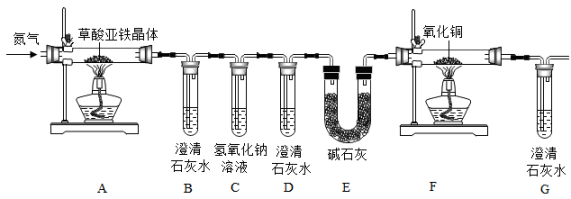
【实验方案】按照上图装置进行实验(夹持装置未画出)。
①试管D中出现浑浊,证明产物中有存在;证明分解产物中存在CO的现象是。
②小明认为应增加H装置,则H装置应放在两个装置之间,若观察到,则证明有水生成;
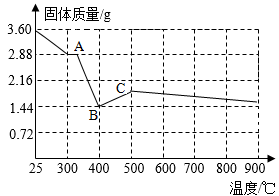
根据图像,若有3.6gFeC2O4•2H2O在敞口环境中充分加热,最终得到红棕色固体1.60g,则该物质的化学式为。由此,你认为进行该实验需要注意的事项是。