
B . 过滤食盐水
B . 过滤食盐水 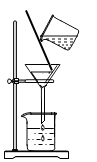
C . 蒸发食盐水
C . 蒸发食盐水 
D . 冷却蒸发皿
D . 冷却蒸发皿 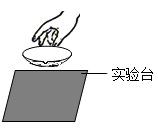
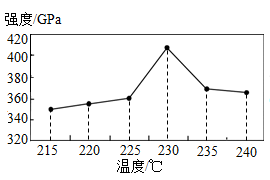
实验1:排水法与排饱和碳酸氢钠法除氯化氢效果的比较
用26%的浓盐酸制取二氧化碳,分别用向上排空气法、排水法、排饱和碳酸氢钠溶液法收集250mL二氧化碳,再各自加入20mL10%的氢氧化钠溶液吸收,再加入10mL18%硝酸溶液调节pH,用氯离子传感器测定氯离子含量。相关数据如图、表1所示:
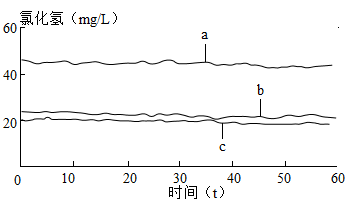
| 1 | 2 | 3 | 三次平均 |
排空集气法 | 23.3 | 20.2 | 46.6 | 29.9 |
排水法 | 3.1 | 3.5 | 3.7 | 3.4 |
排饱和碳酸氢钠法 | 2.6 | 3.2 | 3.0 | 2.9 |
实验2:排水法与排饱和碳酸氢钠溶液法收集二氧化碳纯度的比较
在18℃下,用碳酸钠粉末和稀硫酸制取二氧化碳,分别用上述两种方法收集两瓶250mL的二氧化碳,再各加入20mL10%氢氧化钠溶液,振荡,用压强传感器测定出最终压强如表2。
排水法 | 排饱和碳酸氢钠溶液法 | ||
三次实验所测压强/kpa | 1 | 7.22 | 6.77 |
2 | 7.10 | 6.77 | |
3 | 6.90 | 7.02 | |
平均/kpa | 7.07 | 6.82 | |
已知:实验初始压强为104.40kPa,二氧化碳的纯度计算式为:()×100%
a.加入高锰酸钾固体前先检查装置气密性
b.当导管口有气泡冒出时,开始收集氧气
c.集气瓶中未装满水就开始收集
d.气体收集完毕后,先熄灭酒精灯,再将导管移出水面
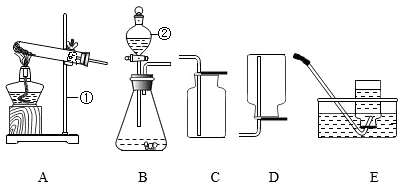
【史料回顾】化学家拉瓦锡在研究水的组成实验时(如图),将水蒸气通过红热的铁管(EF)。

未反应的水蒸气经过S冷凝成液态,流入容器H,产生的气体在K处收集后,经检验证实是氢气,此外还得到一种固体。
【猜想与假设】同学们认为该固体可能是“铁的一种氧化物”,还可能含有“过量的铁”,并模拟上述实验进行如下探究。
【查阅资料】铁有三种氧化物(FeO、Fe2O3、Fe3O4),其中FeO接触到空气会立即由黑色变为红棕色,铁的三种氧化物都不与硫酸铜溶液反应
【实验探究】
实验步骤 | 实验现象 | 实验结论 |
倒出上述反应后的黑色固体,平铺于白纸上 | 黑色固体不变色 | 黑色固体中一定没有(填物质名称) |
取上述黑色固体少许,装入试管,加入足量溶液 | ,且有红色固体出现 | 黑色固体中一定含有 Fe和Fe3O3 |
将水蒸气和空气按一定比例吹入煤气发生炉中与炽热的无烟煤作用产生半水煤气(主要成分是氮气、氢气、一氧化碳、二氧化碳、水)。如图是一种工业上以半水煤气、食盐等为原料制取纯碱的流程。
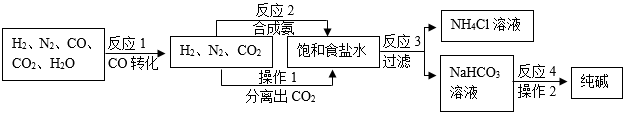
资料:同温同压下,相同体积的气体含有相同的分子数。
①若原料中V(H2):V(CO):V(N2)=19:14:11,则经CO转化后的气体中V(H2):V(N2)=
②反应2中往往先通入NH3 , 然后再通入CO2 , 从溶解性的角度分析,其目的是
③反应3得到的副产品是常见的铵态氮肥,确定该物质是铵盐的方法
④反应4中加热碳酸氢钠晶体可得到纯碱,该反应的化学方程式
【提出问题】一包生石灰干燥剂使用一段时间后,该固体粉末中可能含有哪些物质?
Ⅰ.定性探究固体的成分:
实验步骤 | 实验现象 | 实验结论 |
向烧杯中加入约30mL水,用温度计测定温度t1 , 再向水中加入一定量的该固体粉末,用温度计测定温度t2 | 该固体中含有氧化钙 | |
取上述反应后的混合物,静置,向上层清液中滴加无色酚酞试液 | 无色酚酞变红 | 该固体中含有氢氧化钙 |
向上述混合物中滴加 | 固体消失,有气泡产生 | 该固体中含有碳酸钙 |
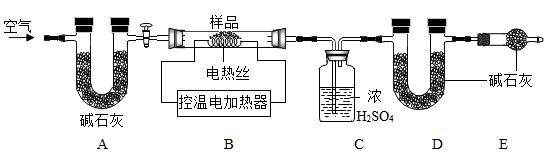
【查阅资料】Ca(OH)2加热至580℃、CaCO3加热至825℃分别分解生成两种氧化物。
【实验步骤】
①实验前首先要,再装入样品。
②连接好装置,先通入一段时间空气,测量装置C、D的质量。
③控温加热使装置B中反应完全,再通一段时间空气,再次测量装置C、D的质量。
①A的作用是,步骤(3)中再通一段时间空气的目的是。
②若装置C、D分别增重9.0g和11.0g,则原固体样品中含有物质。(填化学式)