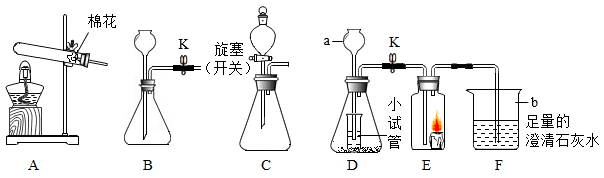

①装置E中蜡烛熄灭,同时装置F中溶液变浑浊,则装置D中化学反应方程式为。从G、H、I中选择收集D产生的气体,可选择的装置有。
②若实验时装置E中蜡烛燃烧更旺,装置D中实验室制备该气体发生的化学反应方程式为:
③装置D中小试管的作用是(填序号)。
a.打开或关闭K时,可以使装置D中的反应随时发生或停止
b.形成液封,防止装置D中产生的气体从长颈漏斗逸出,且节约药品
④实验结束后,要将F中的混合物变得澄清,可用的方法有(填序号)。
a.将混合物过滤 b.向其中加肥皂水 c.向其中加入稀盐酸


写出流程图中电解饱和食盐水的化学反应方程式:

回答下列问题:
①粗盐中含有MgSO4、CaCl2等可溶性杂质,可加入下列物质,利用过滤等操作进行除杂,则加入下列三种物质的先后顺序为(填序号)。
a.适量稀盐酸 b.稍过量的Na2CO3溶液 c.稍过量Ba(OH)2的溶液
②“NaCl+H2O+NH3+CO2═NaHCO3+NH4Cl”是第 II步的反应。下列叙述正确的是。
A.该条件下的溶解度NaHCO3的比NH4Cl大
B.配制饱和精盐水时,可通过搅拌来提高食盐的溶解度
C.向饱和食盐水中先通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收
D.析出晶体后剩余溶液中溶质只有NH4Cl
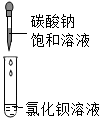
【提出问题】反应后的滤液中含有哪些溶质?
【查阅资料】氯化钠、氯化钡溶液显中性。
明明同学猜想:滤液中溶质是NaCl;
亮亮同学猜想:滤液中溶质是NaCl和(填化学式)的混合物;
红红同学猜想:滤液中溶质是NaCl和Na2CO3的混合物。
取少量滤液于试管中,滴加2﹣3滴无色酚酞溶液,振荡,无明显现象。则猜想不成立。
①明明同学认为要证明亮亮猜想成立也可以改用碳酸钠溶液。你认为明明同学(填“能”或“不能”)达到实验目的。
②红红同学认为要证明亮亮成立也可以改用硝酸银溶液。你认为红红同学(填“能”或“不能”)达到实验目的,原因是。
【归纳与总结】在分析溶液中溶质成分,需要考虑的是生成物,还需考虑反应物是否有剩余。