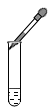
 添加液体
B .
添加液体
B . 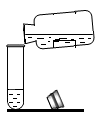 倾倒液体
C .
倾倒液体
C . 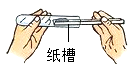 装入粉末状固体
D .
装入粉末状固体
D . 
①取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀A和无色滤液B;
②取少量白色沉淀A于试管中,加入足量的稀盐酸,沉淀部分溶解,并产生无色气体;
③取少量滤液B,向其中通入CO2 , 生白色沉淀
根据以上实验现象,回答下列问题:

【查阅资料】①二氧化碳能溶于水,常温常压下1体积水可溶解1体积的二氧化碳;
②氨气极易溶于水,常温常压下1体积水可溶解700体积的氨气,溶解后形成氨水;
③BaCl2溶液呈中性。
【猜想与假设】猜想一:NaOH 猜想二:猜想三:NaOH和Na2CO3
实验步骤 | 实验现象 | 实验结论 |
①取少量该溶液于试管中,滴入 | 有气泡产生,溶液由红色变为无色 | 猜想一不正确 |
②另取少量该溶液于试管中滴入足量的氯化钡溶液 | 猜想三正确 |
【反思与评价】在分析化学反应后所得物质的成分时,除了考虑生成物外,还需要考虑反应物是否过量,即反应物是否有剩余。
