 B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 



①“金(即钢)柔锡柔,合两柔则刚。”
②何意百炼钢,化为绕指柔(“百炼钢”指生铁经过高温煅烧,反复锤炼成为钢)。
③东晋《抱朴子》中记载:“以曾青涂铁 , 铁赤色如铜”(“曾青”即硫酸铜溶液)。
④美人首饰侯王印,尽是沙中浪底来(“首饰”、“印”指金制品)。
①~④划线部分,发生置换反应的化学方程式为;①说明合金与组成它的纯金属相比,具有的优点是。

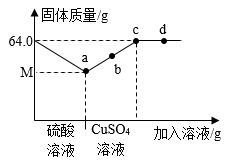
滤液的成分中一定含有的溶质是(填化学式);滤液质量原混合溶液(填“>”、“<”或“=”)。
|
X |
Y |
Z |
|
|
硫酸铜溶液 |
一 |
√ |
√ |
|
稀硫酸 |
一 |
√ |
一 |

①步骤I中反应的化学方程式是。
②除水、AgNO3外,滤液C中还有。(填化学式)
③若经过步骤Ⅳ后得到了43.2g的Ag,则a=。
④如果将步骤I中的Cu原子换成同样个数的Fe原子,则最后得到的Ag的质量(填“会”或“不会”)改变,因为。


猜想一:Al>Cu>R,猜想二:,猜想三:R>Al>Cu。
|
猜想 |
主要操作 |
主要现象 |
实验结论 |
|
一 |
打磨R丝,并将其插入到硫酸铜溶液中 |
R丝表面覆盖了一层红色的物质 |
猜想一 (“成立”或“不成立”) |
|
二 |
打磨粗细相同的R丝、铝丝、铜丝,分别将它们插入到体积相同、溶质质量分数也相同的稀硫酸中 |
①R丝表面产生气泡缓慢,溶液由无色逐渐变成蓝色 ②铝丝表面产生气泡较快 ③铜丝表面没有气泡产生 |
猜想二成立 |
|
三 |
把铝丝插入RSO4溶液中 |
|
猜想三成立 |
(查阅资料)铬(Cr)是银白色有光泽的金属,铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液……铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液……
(预测)三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
(实验过程)取大小相同的三种金属薄片,用砂纸打磨光亮。
|
实验一 |
实验二 |
实验三 |
|
|
实验 方案 |
| | |
| 实验 现象 | 铬片表面产生气泡缓慢,溶液变蓝色。 |
| 铝片表面产生气泡较快。 |
| 结论 | 铬能和稀硫酸发生反应,产生氢气,但反应速率较慢。 | 铜不与稀硫酸反应 |
|
| 三种金属在金属活动性顺序中的相对位置关系是 | |||
(回答问题)
⑴完成上述表格中的空白。
⑵用砂纸打磨金属片的目的是。
⑶实验一所发生反应的化学方程式是。