 B . 配制NaOH溶液
B . 配制NaOH溶液 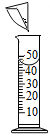 C . 稀释浓H2SO4
C . 稀释浓H2SO4  D . 测稀H2SO4的pH
D . 测稀H2SO4的pH 
 B . 电热水壶
B . 电热水壶  C . 液晶电视
C . 液晶电视  D . 笔记本电脑
D . 笔记本电脑 




A.发芽玉米的提取液中含有a淀粉酶;
B.斐林试剂在加热条件下遇淀粉的消化产物(麦芽糖)会产生砖红色沉淀。
实验操作步骤如下:
步骤一:如图所示操作。
步骤二:把提取液分别倒入同一烧杯的左试管中,摇匀后在原温度下再维持5分钟。
步骤三:分别向各试管加入1毫升斐林试剂,并置于50-60℃水浴中1分钟,观察现象。
实验结果:甲、乙、丙组都出现砖红色沉淀,且乙组比甲、丙的颜色更明显,丁组无砖红色沉淀。
【实验目的】测定过碳酸钠样品(含有的杂质不溶于水且不与酸反应)的纯度。
【实验原理】2Na2CO4+4HCl==4NaCl+2CO2↑+O2↑+2H2O
【实验装置】

【交流与讨论】
Ⅰ.甲同学认为测定产物中O2的体积即可测定样品的纯度,则装置③的作用是:;
Ⅱ.乙同学认为测定产物中CO2的质量(即反应前后装置②的质量差)就可测定样品的纯度。但利用上述实验装置测得CO2的质量并计算样品的纯度,结果会偏高,你认为原因可能是;(填序号)
A.浓盐酸易挥发,产生的氯化氢气体被装置②吸收
B.二氧化碳气体逸出时带出的水蒸气在装置②中冷凝而被吸收
C.产生的气体通过装置②时速度过快
Ⅲ.丙同学提出了一种新方案,得到了大家的一致认可:称取样品12.5g,滴加足量浓盐酸至样品反应完全,再将烧瓶中所有的液体蒸发、结晶、烘干,称得氯化钠固体11.7g。则该样品的纯度为。


【提出猜想】CO2与Na反应可能生成4种物质:C、CO、Na2O和Na2CO3。
【查阅资料】①Na是非常活泼的金属,常温下与O2、H2O等物质反应。
②碱性的Na2CO3溶液与中性的CaCl2溶液发生复分解反应。
③Na2O是白色固体,与H2O反应生成NaOH。
④ 向氯化钯(PdCl2)溶液中通入CO,产生黑色沉淀。
【实验过程】同学们在老师的指导下设计了如下图所示装置(部分夹持仪器已略去)。 
|
序号 |
实验操作 |
主要实验现象 |
实验结论及解释 |
|
打开a,关闭b,由长颈漏斗注入稀盐酸 |
A 中产生大量气泡E中出现浑浊 |
/ |
|
|
当E中出现浑浊时,打开b,关闭a,点燃酒精灯 |
D 中Na剧烈燃烧,产生白烟内壁附着黑色、白色固体G中产生黑色沉淀 |
反应产物有 |
|
|
取D中白色固体于试管中,加水溶解,再加入石灰水 |
产生白色沉淀 |
反应产物还有 |
①实验记录②中,E中出现浑浊再点燃酒精灯的目的是。
②检验第4种物质是否存在的实验方案:取D 中白色固体加足量的水充分溶解并且过滤后,。(将后续操作表述完整)
