|
实验 次数 |
动滑轮重G动/N |
钩码重 G物/N |
钩码上升 高度h物/m |
动力F动/N |
动力作用点移动距离S动/m |
滑轮组的机械效率η |
|
1 |
0.53 |
1 |
0.1 |
0.7 |
0.3 |
47.6% |
|
2 |
2 |
0.1 |
1.1 |
0.3 |
60.6% |
|
|
3 |
4 |
0.1 |
2 |
0.3 |
(一)猜想与假设:
猜想一:固体为CuCO3 , 理由:(用化学反应方程式表示)。
猜想二:固体为Cu(OH)2 , 理由:Na2CO3溶液呈(填“酸”或“碱”)性,能提供大量的离子
猜想三:固体为Cu(OH)2和CuCO3的混合物。
(二)资料查阅:
①Cu(OH)2受热易分解,生成对应的两种氧化物;
CuCO3受热易分解,生成对应的两种氧化物。
②无水CuSO4遇水变蓝。
(三)设计与实验:
⒈将反应后的固、液混合物经(实验操作名称)、洗涤、低温烘干之后,得到蓝色固体。
⒉用下图所示装置,定性探究固体的成分。
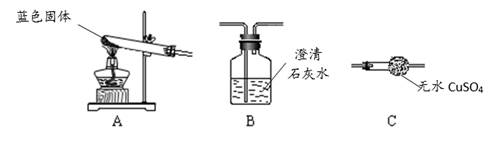
⑴若用装置A、B组合进行实验,B中无现象,则猜想正确;
⑵若用装置A、C组合进行实验,C中无现象,则猜想正确;
⑶小组同学将装置按 A→→(填“B”、“C”)的顺序组合进行实验,验证出猜想三是正确的,那么实验中:B中的现象为,C中的现象为。
结论:固体为Cu(OH)2和CuCO3的混合物。
|
所加盐酸的次数 |
第一次 |
第二次 |
第三次 |
第四次 |
|
盐酸的质量/g |
25 |
25 |
25 |
25 |
|
烧杯及所盛物质总质量/g |
181.2 |
204.4 |
228.6 |
253.6 |
请你据此分析计算:
小资料:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:
2Al+2H2O+2NaOH=2NaAlO2+3H2↑,Fe不与氢氧化钠溶液反应)。
取20g该金属粉末,把100g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量。实验过程中得到的部分数据与如下:
|
加NaOH溶液的次数 |
第一次 |
第二次 |
第三次 |
第四次 |
第五次 |
|
剩余固体的质量/g |
16.4 |
12.8 |
9.2 |
6 |
m |