 称量固体氢氧化钠
B .
称量固体氢氧化钠
B . 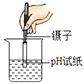 测溶液pH
C .
测溶液pH
C .  过滤
D .
过滤
D .  稀释浓硫酸
稀释浓硫酸
下列环境中的铁制品最容易生锈的是(填字母序号)。
A 未擦干的铁锅 B 涂油漆的栏杆 C 盛水的不锈钢水杯
(探究铁的腐蚀)

该小组进行如下实验:取铁钉用砂纸打磨,称其质量,按上图乙安装装置,放置3天,再取出铁钉称量。在不同温度下重复上述实验,得到铁钉质量增加情况如下表。
|
温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
|
铁钉质量增加/g |
0.02 |
0.04 |
0.08 |
0.16 |
0.18 |
0.18 |
0.18 |
小强同学的实验是探究因素对铁钉腐蚀快慢的影响,结论是。
请分析铁钉质量没有变化的原因:。
用NaOH固体配制20g20%NaOH溶液,无需用到的玻璃仪器有(填标号)。
A 胶头滴管 B 酒精灯 C 量筒 D 烧杯 E 玻璃棒
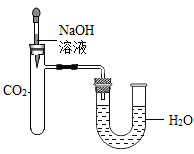
实验前U型管两端液面相平,将NaOH溶液滴入试管中,恢复到室温后,U型管中的液面左高右低。据此,甲同学得出“CO2与NaOH发生了化学反应”的结论。
U型管中液面高度发生变化的原因是。

查阅资料:i.CaCl2溶液呈中性;ii.
实验步骤如下:
①检查装置的气密性,往装置中加入药品;
②关闭K1、K2 , 将注射器中的NaOH溶液缓缓推入A中;
③A中物质充分作用后,打开K1 , B中无色溶液倒吸入A中,A中产生沉淀且溶液显红色
④关闭K1 , 打开K2 , 将注射器活塞向上拉,C中溶液倒吸入A中。
步骤③“产生沉淀”的现象仍不足以证明CO2与NaOH发生了化学反应,理由是。