

|
烧杯编号 |
1 |
2 |
3 |
4 |
|
倒入水的质量/g |
25 |
50 |
100 |
200 |
|
剩余固体情况 |
有 |
有 |
无 |
无 |

(查阅资料)①铁粉在空气中高温加热可以生成四氧化三铁。
②Fe3C空气中高温加热可以生成四氧化三铁和二氧化碳。
(实验装置)

①连接仪器检验气密性;
②在硬质玻璃管内装入5.00样品,并在装置A、B、C中装入相应试剂;
③通入空气至装置B质量不变,记录质量286.04g;
④点燃(填仪器名称)进行实验;
⑤充分反应至装置B质量不变,记录质量286.48g
⑥计算可知样品中Fe3C的质量分数是。
实验中铁粉发生反应的化学方程式是。

a.先停止加热 b.先停止通入空气
c.停止加热或停止通入空气没有先后顺序
①查阅资料:NaHCO3+NaOH=Na2CO3+H2O
②用一定溶质质量分数的 NaHCO3、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考。
|
实验操作 |
NaHCO3溶液 |
NaOH溶液 |
Na2CO3溶液 |
|
加入稀盐酸 |
现象1 |
无明显变化 |
产生气泡 |
|
加入澄清石灰水 |
溶液变浑浊 |
无明显变化 |
现象Ⅱ |
|
加入CaCl2溶液 |
无明显变化 |
溶液变浑浊 |
溶液变浑浊 |
|
加热溶液至沸腾,将气体通入澄清石灰水 |
澄清石灰水变浑浊 |
澄清石灰水无明显变化 |
澄清石灰水无明显变化 |
现象Ⅱ对应反应的化学方程式为。
(实验1)证明反应生成了Na2CO3
同学们选用上表实验中的药品,设计了如图所示实验,先在 NaHCO3溶液中加入A溶液,无明显现象,再加NaOH溶液,溶液变浑浊,则A溶液是。
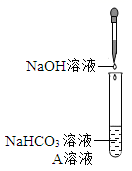
有同学提出这个实验不足以证明有Na2CO3生成,其理由是。为了证明有Na2CO3生成,需要继续进行的操作是。
同学们参考上表中的实验,又设计了一个实验,虽然没有观察到明显的实验现象,但可以证明反应发生了,该实验方案是。
通过实验1和实验2说明,对于没有明显现象的化学反应,可以从两个不同的角度证明反应的发生,这两个角度是。