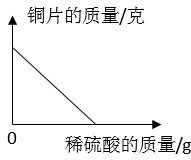
 B .
B .  C .
C . 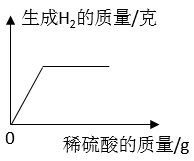 D .
D . 

猜想一:Ca(OH)2溶液与CO2不反应,是CO2溶于水导致瓶内气压变小而变瘪。
猜想二:Ca(OH)2溶液与CO2反应,生成了可溶性物质。
|
实验 |
步骤与操作 |
出实验现象与结果 光 |
结论 |
|
一 |
1.取2个相同的软塑料瓶,分别集满CO2气体,编号为A、B。 |
两瓶内气体无色透明,瓶子形状正常 |
Ca(OH)2溶液与CO2发生了化学反应 |
|
分别向A、B两瓶中加入等量的饱和Ca(OH)2溶液和 ? , 立即拧紧瓶盖并振荡。 |
两瓶内液体未出现浑浊,两瓶均变瘪,A瓶变瘪程度更大。 |
||
|
二 |
测出反应前Ca(OH)2溶液的pH。 |
大于7。 |
|
|
测出反应后A瓶内液体的pH。 |
小于7。 |
甲同学:将镁带和铜粉分别在酒精灯的外焰上加热,观察现象。
乙同学:把铁制容器和铝制容器放在同一潮湿环境中,一段时间后观察容器表面的锈蚀情况。
……
实验后,同学们进行汇报和评价交流。
将CH4气体按如图所示装置进行规范实验,可观察到的实验现象有(填序号);
①A装置中的黑色粉末变成光亮的红色物质
②B装置中的固体由白色变蓝色
③C装置中溶液变浑浊
气体X可能由H2、CH4中的一种或两种组成,同学们按如图所示实验装置对其组成进行探究。

①C装置中溶液变浑浊,可证明气体X中含有;
②根据B装置中的固体由白色变蓝色的现象,得出气体X中含有H2的结论,请对此结论作出评价,并说明理由。
将某火箭燃料X通过如图所示装置,观察到A装置中的黑色粉末变成光亮的红色物质;B装置中的固体由白色变蓝色,C装置中溶液不变浑浊。C中导出的气体是空气中含量最多的物质。已知燃料X是由2种元素组成的纯净物,其相对分子质量为32。根据现象及信息推断并写出:A装置中发生反应的化学方程式为。
建议:①实验可设计4~5组;②实验时每支试管取用硫酸铜溶液5毫升;③每次实验总时间为20分钟。实验室提供铁丝、质量分数为16%的硫酸铜溶液、蒸馏水及其它实验所需的仪器。

【实验步骤】
①取一根玻璃管,用橡皮塞将一端密封;
②将食品脱氧剂粉末迅速装入玻璃管,立即向管口注入一滴水将玻璃管密封,水滴的下端标为A。
弹动玻璃管使脱氧剂粉末分布均匀且紧密,脱氧剂的上端标为O,如图甲所示;
③水平滚动玻璃管,使食品脱氧剂粉末平铺在玻璃管中。静置至水滴不再移动时,水滴的右端标为B,如图乙所示;
④用刻度尺测量出AO段和AB段的长度,并计算出AB
与AO的比值,将数据记录在表格中;
⑤洗涤、干燥实验装置,重复上述实验。
|
实验次数 |
AO/mm |
AB/mm |
AB / AO |
|
1 |
523.5 |
109.5 |
0.2092 |
|
2 |
525.5 |
110.0 |
0.2093 |
|
3 |
527.0 |
110.5 |
0.2097 |
【得出结论】 根据表格中的实验数据, 可知空气中氧气含量为。(用百分数表示)
【思考讨论】
①实验步骤③中,将食品脱氧剂粉末平铺在玻璃管中的目的是。
②实验步骤②中,如果玻璃管内的脱氧剂粉末分布不够紧密,会使实验结果偏大,其原因是。

⑴为了确保水流按预设方向,原水进口和净水出口需要安装单向阀,单向阀类似于人体心脏中心房和心室之间的(填写结构名称)。
⑵为了使水质符合饮用水标准,小金选择了三种滤料去除原水中的杂质,三种滤料的用途如表所示,则滤料甲、乙、丙分别为(按序填写编号)
| 滤料编号 | 用途 |
| ① | 去除水中的泥沙、悬浮物等大颗粒污染物 |
| ② | 去除大分子有机物、重金属离子和细菌等 |
| ③ | 去除残留的细菌、小分子有机物、重金属离子和异味等 |
⑶为了使净水器出水快,需要通过加压装置吸水和压水。下列设计中手柄均可带动活塞做直线往复运动,其中能达到人推拉手柄省力这一目的的是(选填字母)


①氯氟烃分解产生的氯原子在上述反应中起着作用。
②如果某区域上空的臭氧急剧减少,导致该区域内大量生物在短时间内死亡,则该区域生态系统的自动调节能力会发生怎样的变化?
③写出一条保护高空臭氧层的合理建议。。
①如果近地面处臭氧含量过高,将直接导致下列哪一类疾病增加?
A.呼吸道疾病 B.血液传染病 C.糖尿病
②如图是某地8月1日~5日的温度、相对湿度、近地面处臭氧浓度的变化。据图分析,该地这一时段近地面处臭氧浓度的变化与温度的变化是否有关?并阐述理由。