①蒸馏时,先点燃酒精灯,再通冷凝水
②加热氯酸钾和二氧化锰的混合物制备氧气,用排水法收集气体后,先移出导管后撤酒精灯
③实验室制取某气体时,先检查装置气密性后装药品
④分液时,先打开分液漏斗上口的塞子,后打开分液漏斗的旋塞
⑤H2还原CuO实验时,先检验气体纯度后点燃酒精灯
⑥使用托盘天平称盘物体质量时,先放质量较小的砝码,后放质量较大的砝码
⑦蒸馏时加热一段时间,发现忘记加沸石,应迅速补加沸石后继续加热
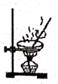 B .
B . 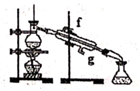 C .
C . 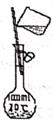 D .
D . 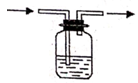
①不慎将浓盐酸洒在桌面上,应立即用浓氢氧化钠溶液冲洗
②不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
③不慎将酸溅到眼中,应立即用大量水冲洗,边洗边眨眼睛
④配制稀硫酸时,可先在量筒中加入一定体积的水,再边搅拌边慢慢加入浓硫酸
⑤不慎将酒精洒到桌面上引起着火,应立即用较多的水浇灭
⑥实验室用剩的白磷直接倒入垃圾箱
⑦浓硫酸不慎沾在皮肤上,应立即用大量水冲洗,最后涂上3%~5%的小苏打溶液
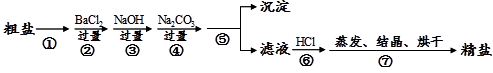

加入试剂b所发生反应的化学方程式为。
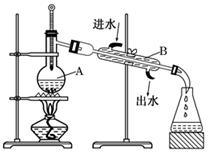
根据图示回答下列问题:
图中两处明显错误是:
①;
②。
B仪器的名称是。
还需要加入少量的,其作用是。
碘是人体不可缺乏的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4 , 该小组先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液,转移到分液漏斗中,再加入一定量的苯,振荡。
分液漏斗使用前应先,振荡后上层液体为(填有机层、水层)。